 2019年江苏省泰州市中考化学试卷含详细答案
2019年江苏省泰州市中考化学试卷含详细答案
《2019年江苏省泰州市中考化学试卷含详细答案》由会员分享,可在线阅读,更多相关《2019年江苏省泰州市中考化学试卷含详细答案(26页珍藏版)》请在七七文库上搜索。
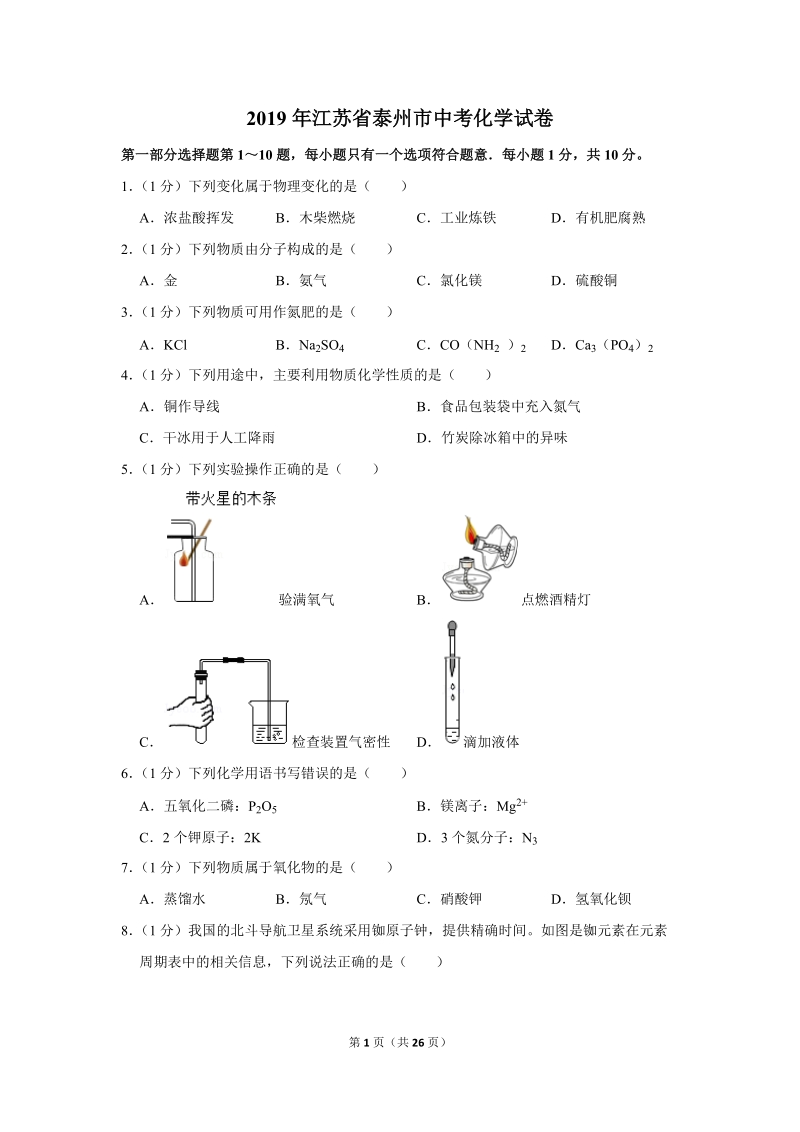
1、第 1 页(共 26 页)2019 年江苏省泰州市中考化学试卷第一部分选择题第 110 题,每小题只有一个选项符合题意每小题 1 分,共 10 分。1 (1 分)下列变化属于物理变化的是( )A浓盐酸挥发 B木柴燃烧 C工业炼铁 D有机肥腐熟2 (1 分)下列物质由分子构成的是( )A金 B氨气 C氯化镁 D硫酸铜3 (1 分)下列物质可用作氮肥的是( )AKCl BNa 2SO4 CCO(NH 2 ) 2 DCa 3(PO 4) 24 (1 分)下列用途中,主要利用物质化学性质的是( )A铜作导线 B食品包装袋中充入氮气C干冰用于人工降雨 D竹炭除冰箱中的异味5 (1 分)下列实验操作正确的
2、是( )A 验满氧气 B 点燃酒精灯C 检查装置气密性 D 滴加液体6 (1 分)下列化学用语书写错误的是( )A五氧化二磷:P 2O5 B镁离子:Mg 2+C2 个钾原子:2K D3 个氮分子: N37 (1 分)下列物质属于氧化物的是( )A蒸馏水 B氖气 C硝酸钾 D氢氧化钡8 (1 分)我国的北斗导航卫星系统采用铷原子钟,提供精确时间。如图是铷元素在元素周期表中的相关信息,下列说法正确的是( )第 2 页(共 26 页)A铷元素属于非金属元素B铷元素的相对原子质量为 85.47gC铷原子的质子数等于中子数D铷元素的原子序数为 379 (1 分)化学与人类健康密切相关,下列说法正确的是(
3、 )A霉变大米经淘洗后可食用B人误食重金属盐中毒,可服蛋清减轻毒性C人体缺锌可引起佝偻病D补充维生素 C 可预防夜盲症10 (1 分)下列说法正确的是( )A将少量面粉和蔗糖分别加入适量的水中,均可形成均一、稳定的混合物B自来水生产过程中加入明矾,目的是杀菌消毒C用氯化钠固体配制 50 克 10%的氯化钠溶液的主要步骤:计算、量取、溶解D向一定体积的气体加压,体积明显变小,可用微粒之间有空隙的性质来解释第 11-15 题,每小题有一个或两个选项符合题意若正确答案包括两个选项只选一个且正确得 1 分;错选得 0 分每小题 2 分,共 10 分11 (2 分)有关物质的组成、构成与性质关系的说法正
4、确的是( )A水和过氧化氢组成元素相同,故它们的化学性质相同B稀硫酸和盐酸溶液中都含有大量氢离子,故它们具有一些共同的化学性质C构成金刚石和石墨的原子相同但排列方式不同,故它们的物理性质不同D氢氧化铜和氢氧化钠都含有氢氧根离子,故它们都能使无色酚酞试液变红色12 (2 分)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )第 3 页(共 26 页)At 1时,甲、乙两物质的溶解度大小关系:甲乙Bt 2时,等质量的甲、乙溶液中,溶剂的质量一定相等Ct 3时,若将 N 点的甲溶液转变为 M 点的甲溶液,可采取恒温蒸发溶剂的方法D将 t1时甲、乙的饱和溶液升温至 t3,所得甲、乙的溶液仍都
5、是饱和溶液13 (2 分)下列说法正确的是( )A制作烟花常加入镁粉,原因是镁燃烧能发出耀眼的白光B通常情况下铝制品耐腐蚀,原因是铝不易发生化学反应C巴黎圣母院失火,消防队员用水灭火是为了降低可燃物的着火点D实验时,氯酸钾中加入少量高锰酸钾加热,发现产生氧气的速率加快,原因是高锰酸钾对氯酸钾分解起催化作用14 (2 分)下列有关物质的检验、鉴别以及分离、提纯的做法,正确的是( )A检验食品中是否含有淀粉:用碘化钾溶液B鉴别 K2SO4 和(NH 4) 2SO4 两种固体:加熟石灰研磨C除去 CaCO3 固体中的少量 Na2CO3:加入足量稀盐酸充分反应后过滤D分离 Fe 和 CuSO4 固体混
6、合物:加入足量的水溶解,过滤15 (2 分)某化学兴趣小组进行了两组实验。实验一:如图 1,将除去表面氧化膜的锌片插入到盛 CuSO4 溶液的烧杯中;实验二:如图 2,用导线将除去表面氧化膜的铜片和锌片分别连接到电流表的正、负极,然后把铜片和锌片一起插入盛 CuSO4 溶液的烧杯中。下列说法正确的是( )第 4 页(共 26 页)A实验一观察到锌表面有红色物质析出,反应后溶液质量会减小B实验二观察到电流表指针发生了偏转C实验一和实验二都明显体现了化学能转化为电能D实验一和实验二从微观角度分析,都存在着电子的得失二、非选择题(共 40 分16 (7 分)化学与科技、生产、生活密切相关。(1)某学
7、校的营养早餐配料标签如图 1 所示,该配料中富含油脂的物质是 。当衣服上粘有油脂时,可以用洗衣粉除去,其去污原理是 。(2)泰州是中国人民解放军海军的摇篮,138 泰州舰上使用的玻璃钢属于 材料;舰体在高盐的海水中易生锈,原因是海水中所含的 物质存在时会加速铁的锈蚀。(3)利用植物秸秆、牲畜粪便等可制得沼气,沼气的主要成分甲烷在空气中完全燃烧的化学方程式为 ,推广使用沼气做燃料的优点是 (答 1 点即可) 。(4)一种创可贴中间有个凸起的小囊区,如图 2按贴伤口的同时,小囊区内的水和硝酸铵固体被挤破混合,利用硝酸铵固体溶解时温度 ,起到快速止血的作用。17 (8 分)请回答下列实验问题:(1)
8、现提供下列装置:如图 E 装置中,甲仪器的名称是 。实验室用 KClO3 和 MnO2 混合制 O2,发生装置可选用 (填装置序号) ,用装第 5 页(共 26 页)置 C 干燥 O2,气体由导管 端(填“a”或“b” )进入,用 E 装置收集 O2 的依据是 。英国化学家布莱克是第一个“捕捉”到 CO2 的人,实验室制备 CO2 的化学方程式为 ;1774 年德国化学家贝格曼将 CO2 通入紫色石蕊试液中,发现试液由紫色变为红色,此反应的化学方程式为 。(2)对一定质量的粗盐(含泥沙)进行初步提纯。实验的主要步骤:称量与溶解、过滤、蒸发;蒸发结束后用 (填仪器名称)将固体从蒸发皿转移到纸片上
9、,比较食盐提纯前后的状态。下列有关蒸发过程说法正确的是 (填序号)a蒸发时用玻璃棒不断搅拌b当蒸发皿中水分全部蒸干时,停止加热c蒸发时若有滤液溅出,则精盐质量将偏低d蒸发过程中,溶液中钠元素质量增大18 (8 分)AJ 是初中化学常见的物质,A 是一种含有四种元素的盐,可用作治疗胃酸过多,其反应原理:A 和 B 反应生成 C、D 和 E 三种物质,通过光合作用 D 和 E 反应生成 F 和 G,煤气主要成分 H 在 F 中燃烧生成 E,I 和 D 反应只生成 J,J 常用于改良酸性土壤。(1)G 的化学式为 , G 中质量分数最大的元素是 。(2)A 的俗称是 ;A 和 B 反应的化学方程式为
10、 ,基本反应类型是 。(3)I 的用途是 (答 1 点即可) ;H 在 F 中燃烧的化学方程式为 。(4)改良后土壤浸出液的酸碱度可用 测定。19 (10 分)某化学兴趣小组学习了酸、碱、盐的知识后,对某些盐的性质开展了探究活动。研究主题:探究 FeC13 溶液加热、灼烧的变化相关信息:酒精(C 2H5OH)具有还原性,加热条件下能与 Fe2O3 反应;Fe 和 Fe3O4 易被磁铁吸引,FeO 是一种黑色固体,不能被磁铁吸引; Fe3O4 能与盐酸反应,生成盐和水。(1)实验一:将大约 20mL 饱和 FeCl3 溶液在蒸发皿中加热蒸发,沸腾后发现溶液中逐渐产生红褐色浑浊。第 6 页(共 2
11、6 页)FeCl3 溶液呈黄色主要是因为溶液中含有铁离子,铁离子符号为 。加热时, FeCl3 易与水反应生成红褐色物质和盐酸,反应的化学方程式: 。由实验启示,FeCl 3 溶液通过蒸发结晶的方式 (填“能”或“不能” )获得FeCl3 固体。(2)实验二:将实验一蒸发获得的红褐色固体转移到坩埚中灼烧,颜色由红褐色变为红棕色。此过程发生分解反应,除生成红棕色物质外,还生成水,反应的化学方程式: 。氢氧化镁、氢氧化铜等加热分解也能得到对应的金属氧化物,结合实验,从物质类别及其溶解性推断,通过加热分解 可生成对应的金属氧化物。(3)实验三:小组同学用多根玻璃棒蘸取饱和 FeCl3 溶液于酒精灯火
12、焰上灼烧,随着加热时间的持续,在 1 分钟内观察到玻璃棒表面颜色的变化依次为:黄色、红褐色、红棕色、黑色。实验三相对于实验一和二,优点是 (答 1 点即可) 。同学们对黑色物质的成分产生了疑问。联系酒精的可燃性、还原性等相关性质,对黑色物质的成分提出了猜想,经讨论认为,可能是 和 Fe3O4 四种物质中的一种或几种。为了确定黑色物质的成分,收集黑色物质,进行了如下实验:实验步骤 实验现象 实验结论取黑色粉末,用磁铁吸引,观察现象 黑色粉末全部被磁铁吸引向装有黑色粉末的试管中加入足量的盐酸,充分反应,观察现象固体逐渐溶解,但无气泡产生综合实验现象判断,此黑色物质成分是 (4)拓展延伸配制 FeC
13、l3 溶液时,为防止出现红褐色物质,可向其中滴加少量的 溶液。结合已学知识,从元素化合价变化的角度分析,Fe 2O3 发生还原反应时,反应前后铁元素化合价一般呈 (填“上升”或“下降” )的变化。20 (7 分)钼是一种重要的金属,用它制成的合金有良好的机械性能,在工农业生产和国防上都有广泛的用途。如图是利用钼矿石(主要成分为 MoS2)制备金属钼的流程图:第 7 页(共 26 页)信息:MoO 3+3H2 Mo+3H2O请回答下列问题:(1)反应 常将钼矿石粉碎,目的是 ;MoO 3 中钼元素的化合价为 。(2)操作的名称是 ;常用 NaOH 溶液吸收反应 的尾气,化学方程式为 。(3)制得
14、 19.2 吨金属钼,理论上至少需含 MoO380%的粗产品多少吨?请写出计算过程。注:粗产品杂质中不含钼元素第 8 页(共 26 页)2019 年江苏省泰州市中考化学试卷参考答案与试题解析第一部分选择题第 110 题,每小题只有一个选项符合题意每小题 1 分,共 10 分。1 (1 分)下列变化属于物理变化的是( )A浓盐酸挥发 B木柴燃烧 C工业炼铁 D有机肥腐熟【分析】有新物质生成的变化叫化学变化,木柴燃烧、都属于化学变化;没有新物质生成的变化叫物理变化。化学变化的特征是:有新物质生成。判断物理变化和化学变化的依据是:是否有新物质生成。【解答】解:A、浓盐酸挥发没有新物质生成,属于物理变
15、化;故选项正确;B、木柴燃烧生成二氧化碳等,属于化学变化;故选项错误;C、工业炼铁,铁是新物质,属于化学变化;故选项错误;D、有机肥腐熟生成新物质,属于化学变化;故选项错误;故选:A。【点评】本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否有新物质生成,问题就很容易解决。本考点主要出现在选择题和填空题中。2 (1 分)下列物质由分子构成的是( )A金 B氨气 C氯化镁 D硫酸铜【分析】根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是由分子构成的,气态的非金属单质和一般由非金属元素组成的化合物,如氢气、水等;有些物质是由离子构成的,一般是含有金属元素和非金
16、属元素的化合物,如氯化钠,进行分析判断即可。【解答】解:A、金属于金属单质,是由铁原子直接构成的,故选项错误。B、氨气是由非金属元素组成的化合物,是由氨分子构成的,故选项正确。C、氯化镁是含有金属元素和非金属元素的化合物,氯化镁是由钠离子和氯离子构成的,故选项错误。D、硫酸铜是含有金属元素和非金属元素的化合物,硫酸铜是由铜离子和硫酸根离子构成的,故选项错误。故选:B。【点评】本题难度不大,主要考查了构成物质的微观粒子方面的知识,对物质进行分类第 9 页(共 26 页)与对号入座、掌握常见物质的粒子构成是正确解答本题的关键。3 (1 分)下列物质可用作氮肥的是( )AKCl BNa 2SO4 C
17、CO(NH 2 ) 2 DCa 3(PO 4) 2【分析】含有氮元素的肥料称为氮肥,含有磷元素的肥料称为磷肥,含有钾元素的肥料称为钾肥,同时含有氮、磷、钾三种元素中的两种或两种以上的肥料称为复合肥。【解答】解:A、KCl 中含有钾元素,属于钾肥,故 A 错。B、Na 2SO4 不含有营养元素,不属于化肥,故 B 错。C、CO(NH 2 ) 2 中含有氮元素,属于氮肥,故 C 正确。D、Ca 3(PO 4)中含有磷元素,属于磷肥,故 D 错。故选:C。【点评】本题主要考查化肥的分类方面的知识,解答时要分析化肥中含有哪些营养元素,然后再根据化肥的分类方法确定化肥的种类。4 (1 分)下列用途中,主
18、要利用物质化学性质的是( )A铜作导线 B食品包装袋中充入氮气C干冰用于人工降雨 D竹炭除冰箱中的异味【分析】物质在化学变化中表现出来的性质叫化学性质,如可燃性、助燃性、氧化性、还原性、酸碱性、稳定性等;物质不需要发生化学变化就表现出来的性质,叫物理性质;物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、导热性、溶解性、挥发性、吸附性等。【解答】解:A、铜作导线是利用铜的导电性,属于物理性质;故选项错误;B、食品包装袋中充入氮气是利用氮气的稳定性,属于化学性质;故选项正确;C、干冰用于人工降雨是利用干冰吸热升华,属于物理性质;故选项错误;D、竹炭除冰箱中的异味是利用碳的吸附
19、性,属于物理性质;故选项错误;故选:B。【点评】本考点考查了物理性质和化学性质的区分,要记忆有关铜、氮气、干冰、竹炭的性质,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中。5 (1 分)下列实验操作正确的是( )第 10 页(共 26 页)A 验满氧气 B 点燃酒精灯C 检查装置气密性 D 滴加液体【分析】A、氧气验满要放在集气瓶口; B、点燃酒精灯要用火柴点燃,不能引燃;C、检查装置气密性要在密封体系内;D 、根据胶头滴管的使用方法考虑。【解答】解:A、氧气验满要将带火星的木条放在集气瓶口,故 A 错;B、点燃酒精灯要用火柴点燃,不能引燃,故 B 错;C、检查
20、装置气密性要在密封体系内,故 C 正确;D、胶头滴管要垂悬在试管口上方,故 D 错。故选:C。【点评】解答本题关键是熟悉实验基本操作,防止错误操作造成实验失败。6 (1 分)下列化学用语书写错误的是( )A五氧化二磷:P 2O5 B镁离子:Mg 2+C2 个钾原子:2K D3 个氮分子: N3【分析】A、化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,进行分析判断。B、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带 1 个电荷时,1 要省略。C、原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在
21、其元素符号前加上相应的数字。D、分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字。【解答】解:A、五氧化二磷的化学式为 P2O5,故选项化学用语书写正确。B、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷第 11 页(共 26 页)数,数字在前,正负符号在后,带 1 个电荷时,1 要省略。镁离子可表示为 Mg2+,故选项化学用语书写正确。C、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故 2 个钾原子表示为:2K ,故选项化学用语书写正确。D、由分子的表示方法,正确书写物质的化学式,表
22、示多个该分子,就在其分子符号前加上相应的数字,则三个氮分子可表示为:3N 2,故选项化学用语书写错误。故选:D。【点评】本题难度不大,掌握常见化学用语(原子符号、分子符号、化学式、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键。7 (1 分)下列物质属于氧化物的是( )A蒸馏水 B氖气 C硝酸钾 D氢氧化钡【分析】本题考查氧化物的识别,根据氧化物的概念可知氧化物只有两种元素,且必须有氧元素。【解答】解:A 中有两种元素,其一为氧元素,属于氧化物,故 A 正确。B 中有一种元素,属于单质,故 B 错。C 中有三种元素,也含氧元素,但不属于氧化物,属于盐,故 C 错
23、误。D 中有三种元素,也含氧元素,但不属于氧化物,属于碱,故 D 错误。故选:A。【点评】本题较简单,主要从概念上来抓住判断的关键点,两个关键点缺一不可,要同时具备。8 (1 分)我国的北斗导航卫星系统采用铷原子钟,提供精确时间。如图是铷元素在元素周期表中的相关信息,下列说法正确的是( )A铷元素属于非金属元素B铷元素的相对原子质量为 85.47gC铷原子的质子数等于中子数D铷元素的原子序数为 37第 12 页(共 26 页)【分析】根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。【
24、解答】解:A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名称是铷,带“钅”字旁,属于金属元素,故选项说法错误。B、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为 85.47,相对原子质量单位是“1” ,不是“克” ,故选项说法错误。C、铷原子的质子数不等于中子数,故选项说法错误。D、根据元素周期表中的一格可知,左上角的数字为 37,该元素的原子序数为 37,故选项说法正确。故选:D。【点评】本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)进行分析解题的能力。9 (1 分)化学与人类健康密切相


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2019 江苏省 泰州市 中考 化学 试卷 详细 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-84900.html