 2019年重庆市中考第一轮基础知识《第14讲:溶液含溶质质量分数的计算》同步练习(含答案)
2019年重庆市中考第一轮基础知识《第14讲:溶液含溶质质量分数的计算》同步练习(含答案)
《2019年重庆市中考第一轮基础知识《第14讲:溶液含溶质质量分数的计算》同步练习(含答案)》由会员分享,可在线阅读,更多相关《2019年重庆市中考第一轮基础知识《第14讲:溶液含溶质质量分数的计算》同步练习(含答案)(10页珍藏版)》请在七七文库上搜索。
1、第 14 讲 溶液(含溶质质量分数的计算)(时间 :50 分钟 分值:66 分)基础过关一、选择题1. (2017 桂林)下列物质在水中,能形成溶液的是( )A. 牛奶 B. 汽油 C. 泥土 D. 味精2. (2017 无锡)在盛有水的烧杯中加入以下某种物质,形成溶液的过程中,温度下降。这种物质可能是( )A. 氯化钠 B. 硝酸铵C. 氢氧化钠 D. 蔗糖3. (2017 重庆一中期中)下列操作方法中,利用乳化作用的是( )A. 用煮沸软化硬水B. 用汽油清洗油污C. 用洗涤剂清洗油污D. 用酒精除去碘单质4. (2017 贺州) 下列有关溶液的说法,正确的是( )A. 溶液一定是无色透明
2、的B. 碘酒的溶剂是乙醇C. 溶质一定是固体D. 浓溶液一定是饱和溶液5. (2017 重庆育才中学模拟)下列有关溶液的说法不正确的是( )A. 溶液中的溶质可能是多种B. 不饱和溶液也可能是浓溶液C. 均一、稳定的液体一定是溶液D. 饱和溶液析出晶体后,溶质质量分数可能不变6. (2017 聊城)下列关于溶液说法正确的是( )A. 把氯化钠和植物油放入水中,充分搅拌后都能形成溶液B. 把 20%的蔗糖溶液均分成两份,每份溶液的溶质质量分数为 10%C. 向 20 时的蔗糖饱和溶液中加入食盐,食盐不再溶解D. 配制 50 g 16%的氯化钠溶液一般经过计算、称量(或量取)、溶解、装瓶存放等步骤
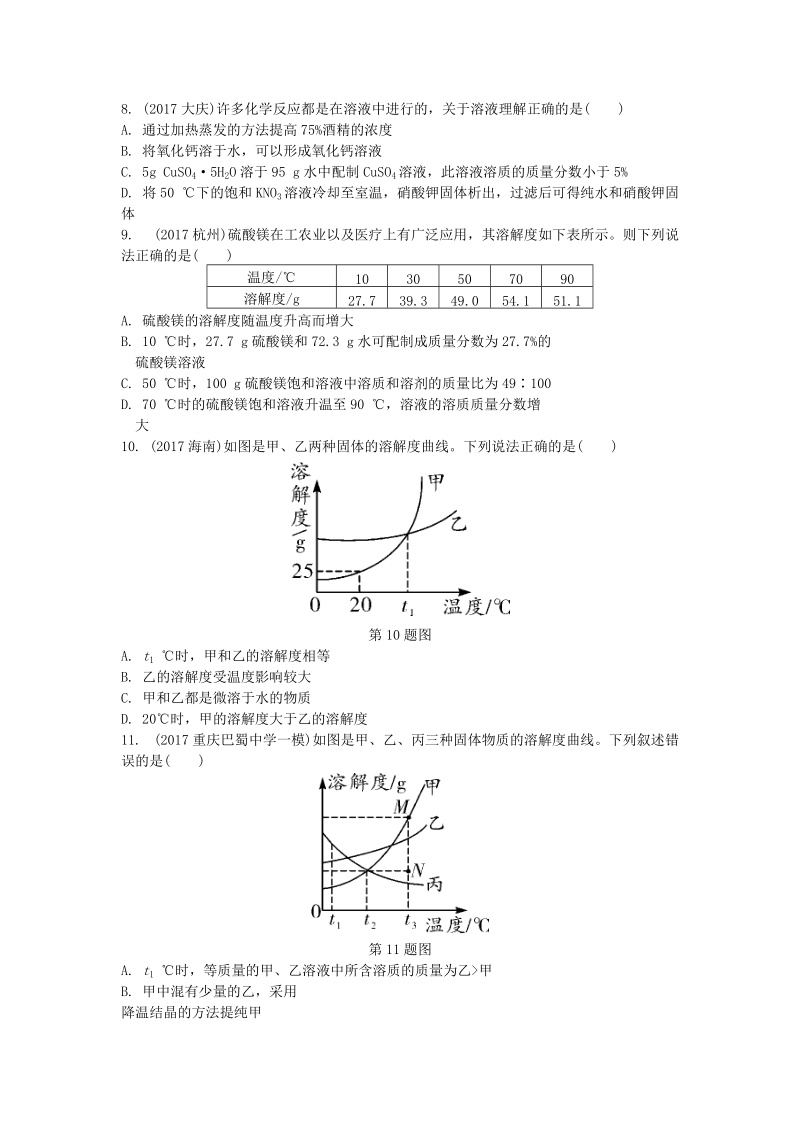
3、7. (2017 重庆江津中学一模)如图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质 t1 时的饱和溶液升温至 t2 ,所得溶液的溶质质量分数关系正确的是( )第 7 题图A. 甲乙丙 B. 甲乙丙C. 甲乙丙 D. 乙甲丙8. (2017 大庆)许多化学反应都是在溶液中进行的,关于溶液理解正确的是( )A. 通过加热蒸发的方法提高 75%酒精的浓度B. 将氧化钙溶于水,可以形成氧化钙溶液C. 5g CuSO45H2O 溶于 95 g 水中配制 CuSO4溶液,此溶液溶质的质量分数小于 5%D. 将 50 下的饱和 KNO3溶液冷却至室温,硝酸钾固体析出,过滤后可得纯水和硝酸钾固体9
4、. (2017 杭州)硫酸镁在工农业以及医疗上有广泛应用,其溶解度如下表所示。则下列说法正确的是( )温度/ 10 30 50 70 90溶解度/g 27.7 39.3 49.0 54.1 51.1A. 硫酸镁的溶解度随温度升高而增大B. 10 时,27.7 g 硫酸镁和 72.3 g 水可配制成质量分数为 27.7%的硫酸镁溶液C. 50 时,100 g 硫酸镁饱和溶液中溶质和溶剂的质量比为 49100D. 70 时的硫酸镁饱和溶液升温至 90 ,溶液的溶质质量分数增大10. (2017 海南)如图是甲、乙两种固体的溶解度曲线。下列说法正确的是( )第 10 题图A. t1 时,甲和乙的溶解
5、度相等B. 乙的溶解度受温度影响较大C. 甲和乙都是微溶于水的物质D. 20时,甲的溶解度大于乙的溶解度11. (2017 重庆巴蜀中学一模)如图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述错误的是( )第 11 题图A. t1 时,等质量的甲、乙溶液中所含溶质的质量为乙甲B. 甲中混有少量的乙,采用降温结晶的方法提纯甲C. 若要将 N 点的甲溶液转变为 M 点的甲溶液,可采取恒温蒸发溶剂的方法D. t3 时,将甲、乙、丙三种物质的饱和溶液降温至 t2 ,所得溶液溶质质量分数的大小关系为乙甲丙二、填空题12. (2017 毕节)(3 分)根据下表中 NaCl 和 KNO3部分溶解度数据分析,
6、回答下列问题:温度/ 0 10 20 30 40 50 60NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3溶解度/gKNO3 13.3 20.9 31.6 45.8 63.9 85.5 110(1)30 时,NaCl 的溶解度是_g。(2)NaCl 与 KNO3相比较,溶解度受温度变化影响较小的物质是_。(3)20 时,在 100 g 水中加入 50 g NaCl 或 50 g KNO3,充分搅拌后,将溶液温度升高到 40 (不考虑水分蒸发),所得溶液是不饱和溶液,则加入的物质是_。13. (2017 河南)(3 分)如图是甲、乙两种固体的溶解度曲线。将 t2
7、时相同质量的甲、第 13 题图乙两种饱和溶液降温至 t1 ,只有甲的溶液中有固体析出,则乙的溶解度曲线为_(填“X”或“Y”);甲和乙溶解度相等时的温度为_; t3 时,将 30 g甲的饱和溶液稀释为质量分数为 10%的溶液,需加水的质量为_g。 14. (2017 重庆江津中学一模)(6 分)甲、乙、丙三种物质的溶解度曲线如图所示,根据图中信息回答下列问题:第 14 题图(1)50 时,乙物质的溶解度是_g。(2)当甲中含有少量乙时,提纯甲的方法是_。(3)要使 50 时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是_。(4)50 时,将 40 g 乙物质放入 88 g 水中充分
8、溶解后,所得溶液的溶质质量分数为_(精确到 0.1%)。(5)50 时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至 10 ,析出晶体最多的是_,所得溶液的溶质质量分数由大到小的顺序为_。15. (2017 陕西)(4 分)下表是 NaCl 和 KNO3在不同温度时的溶解度,回答问题。温度/ 10 20 30 40 50 60NaCl 35.8 36.0 36.3 36.6 37.0 37.3溶解度/g KNO3 20.9 31.6 45.8 63.9 85.5 110.0(1)两种物质中,溶解度受温度影响变化较大的是_。(2)60 时,按图示操作:第 15 题图A 中溶液是_(填“饱和”
9、或“不饱和”)溶液,C 中溶液的总质量是_g。(3)50时,将两种物质的饱和溶液各 100 g,分别加热蒸发 10 g 水后,再恢复到 50 ,剩余溶液的质量:NaCl 溶液_(填“大于”、“等于”或“小于”)KNO 3溶液。三、计算题16. (6 分)取硫酸钠和氯化钠的混合物 15 g,加入 180 g 水使其完全溶解,再加入 100 g 氯化钡溶液恰好完全反应,过滤,得到 271.7 g 滤液(不考虑实验过程中质量损失)。计算:(1)该混合物中硫酸钠的质量分数(计算结果精确到 0.1%);(2)反应后所得滤液中溶质的质量分数(计算结果精确到 0.1%)。 满分冲关一、选择题1. (2017
10、 广州)下列说法不正确的是( )A. 硝酸铵固体溶于水是吸热过程B. 乙醇与水混合可形成溶液C. 饱和溶液的质量分数一定大于不饱和溶液D. 氯化钠溶液能够导电是因为溶液中存在自由移动的离子 2. (2017 昆明)如图是甲、乙两物质的溶解度曲线。下列说法正确的是( )第 2 题图A. t2 时,甲的溶解度为 50B. 甲、乙的溶解度都随温度的升高而增大C. 将甲溶液从 t2 降温至 t1 ,一定有晶体析出D. t1 时,甲、乙两种饱和溶液的溶质质量分数相等 3. (2017 兰州 ) 如图所示,装置气密性良好,广口瓶内装有某种固体,向其中滴加某种液体后,U 形管内液面 a 低于 b,不符合上述
11、实验现象的一组试剂是( )第 3 题图A. 生石灰和水 B. 铁粉和稀盐酸C. 硝酸铵和水 D. 纯碱和稀盐酸二、填空题4. (2017 重庆南开中学期中)(4 分)根据如图 A、B、C 三种固体的溶解度曲线回答:(A、B、C 析出晶体时均不含结晶水)(1)在 t1 时,A 的溶解度为_。第 4 题图(2)要使 t1 的 A 的接近饱和的溶液成为饱和溶液,可采用的方法是_(答一条即可)。(3)在 t2 时,配制等质量的各溶质的饱和溶液,需水的质量最多的是_(填字母)。(4)将等质量 t2 时的 A、B、C 饱和溶液分别恒温蒸发相同质量的水,所得溶液质量从大到小的关系是_。5. (2017 兰州
12、)(5 分) 甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:第 5 题图(1)t1 时,甲、乙两种物质的溶解度大小关系为甲_乙(填“”、“”或“”)。(2)P 点的含义_。(3)t2 时,把 20 g 固体甲放入 50 g 水中,充分搅拌,所得溶液的质量是_g。(4)欲将 t2 时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是_。(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用_的方法。6. (2017 株洲)(3 分)如图为甲和乙两种固体物质的溶解度曲线。回答下列问题:第 6 题图(1)t1时,两种物质的饱和溶液中溶质的质量分数较大的是_。(2)要将 t2时甲的饱和
13、溶液变成不饱和溶液,可采取的措施有:增加溶剂、_等。(3)t2时,在盛有 120 g 蒸馏水的烧杯中,加入 80 g 甲固体,充分溶解后,所得溶液中溶质的质量分数为_。7. (2017 武汉)(4 分)R 是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图 1所示。某化学兴趣小组的同学进行了如图 2 所示实验。第 7 题图(1)t1 时,氯化铵的溶解度为_g。(2)的溶液中溶质质量分数为_。(3)根据以上信息可推出 R 是_(写名称或化学式均可)。(4)关于图 2 中烧杯内的物质,以下几种说法正确的有_。A. 、中,只有中上层清液是饱和溶液B. 若使中的固体溶解,可采用加水或升温的方法C
14、. 和的溶液中,溶质质量相等D. 的溶液中溶质质量分数一定比的上层清液中溶质质量分数小答案基础过关1. D 【解析】牛奶不溶于水,形成的是乳浊液,A 错误;汽油不溶于水,形成的混合物不均一、不稳定,长时间放置会分层,B 错误;泥土不能溶于水,形成的混合物不均一、不稳定,长时间放置会有沉淀产生,属于悬浊液,C 错误;味精能溶于水,形成的是均一、稳定的混合物,D 正确。2. B 【解析】氯化钠和蔗糖溶于水,所得溶液温度无明显变化;硝酸铵溶于水,所得溶液温度降低,氢氧化钠溶于水,所得溶液温度升高。故选 B。3. C 【解析】煮沸时水中可溶性钙镁离子转化为沉淀除去,使硬水软化;用汽油洗去油污利用的是汽


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2019 重庆市 中考 第一轮 基础知识 14 溶液 溶质 质量 分数 计算 同步 练习 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-62727.html