 2019年高考化学二轮复习专题16《盐类水解溶解平衡》教案
2019年高考化学二轮复习专题16《盐类水解溶解平衡》教案
《2019年高考化学二轮复习专题16《盐类水解溶解平衡》教案》由会员分享,可在线阅读,更多相关《2019年高考化学二轮复习专题16《盐类水解溶解平衡》教案(15页珍藏版)》请在七七文库上搜索。
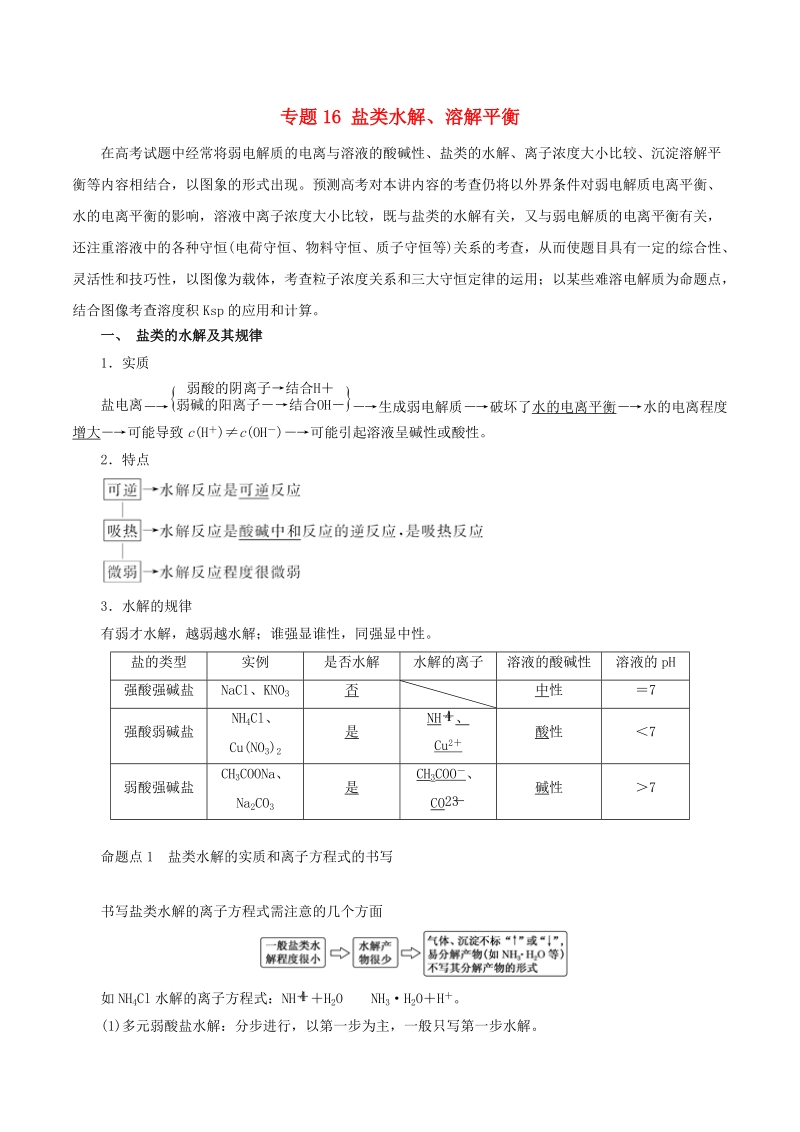
1、专题 16 盐类水解、溶解平衡在高考试题中经常将弱电解质的电离与溶液的酸碱性、盐类的水解、离子浓度大小比较、沉淀溶解平衡等内容相结合,以图象的形式出现。预测高考对本讲内容的考查仍将以外界条件对弱电解质电离平衡、水的电离平衡的影响,溶液中离子浓度大小比较,既与盐类的水解有关,又与弱电解质的电离平衡有关,还注重溶液中的各种守恒(电荷守恒、物料守恒、质子守恒等)关系的考查,从而使题目具有一定的综合性、灵活性和技巧性,以图像为载体,考查粒子浓度关系和三大守恒定律的运用;以某些难溶电解质为命题点,结合图像考查溶度积 Ksp 的应用和计算。一、 盐类的水解及其规律1实质 生成弱电解质 破坏了水的电离平衡
2、水的电离程度盐 电 离 弱 酸 的 阴 离 子 结 合 H弱 碱 的 阳 离 子 结 合 OH 增大 可能导致 c(H ) c(OH ) 可能引起溶液呈碱性或酸性。2特点3水解的规律有弱才水解,越弱越水解;谁强显谁性,同强显中性。盐的类型 实例 是否水解 水解的离子 溶液的酸碱性 溶液的 pH强酸强碱盐 NaCl、KNO 3 否 中性 7强酸弱碱盐NH4Cl、Cu(NO3)2是NH 、 4Cu2酸性 7弱酸强碱盐CH3COONa、Na2CO3是CH3COO 、CO23碱性 7命题点 1 盐类水解的实质和离子方程式的书写书写盐类水解的离子方程式需注意的几个方面如 NH4Cl 水解的离子方程式:N
3、H H 2ONH 3H2OH 。 4(1)多元弱酸盐水解:分步进行,以第一步为主,一般只写第一步水解。如 Na2CO3水解的离子方程式:CO H 2OHCO OH 。23 3(2)多元弱碱盐水解:离子方程式一步写完。如 FeCl3水解的离子方程式:Fe 3 3H 2OFe(OH) 33H 。(3)阴、阳离子相互促进水解,水解程度较大,书写时要用“= =”、 “” 、 “”等。如 NaHCO3与 AlCl3混合溶液反应的离子方程式:Al 3 3HCO =Al(OH)33CO 2。 3例 1在盐类发生水解的过程中,正确的说法是( )A盐的电离平衡被破坏B水的电离程度逐渐增大C溶液的 pH 发生了较
4、大改变D水解后溶液一定呈酸性或碱性【答案】B 例 2下列水解的离子方程式正确的是( )AHCO H 2OCO 2OH 3BS 2 2H 2OH 2S2OH CFe 3 3H 2OFe(OH) 33H DCO H 2OHCO OH 23 3【答案】D 【解析】一般盐类水解程度很小,所以通常不放出气体或生成沉淀,即 A、C 选项错误;对于多元弱酸酸根离子应分步水解,B 选项错误,D 选项正确。命题点 2 盐类水解的规律及其应用1 “谁弱谁水解,越弱越水解” 。如酸性:HCNCH 3COONa。2强酸的酸式盐只电离,不水解,溶液显酸性。如 NaHSO4在水溶液中:NaHSO 4=Na H SO 。2
5、43弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。(1)若电离程度小于水解程度,溶液呈碱性。如 NaHCO3溶液中:HCO H CO (次要), 3 23HCO H 2OH 2CO3OH (主要)。 3(2)若电离程度大于水解程度,溶液显酸性。如 NaHSO3溶液中:HSO H SO (主要), 3 23HSO H 2OH 2SO3OH (次要)。 34相同条件下的水解程度:正盐相应酸式盐,如 CO HCO 。23 35相互促进水解的盐单独水解的盐水解相互 抑制的盐。如 NH 的水解:(NH 4)2CO3(NH4) 42SO4(NH4)2Fe(SO4)2。例 32
6、5 时,浓度均为 0.2 mol/L 的 NaHCO3和 Na2CO3溶液中,下列判断不正确的是( )A均存在电离平衡和水解平衡B存在的粒子种类相同C c(OH )前者大于后者D分别加入 NaOH 固体,恢复到原温度, c(CO )均增大23【答案】C 例 4有四种物质的量浓度相等且都由一价阳离子 A 和 B 及一价阴离子 X 和 Y 组成的盐溶液。据测定常温下 AX 和 BY 溶液的 pH7,AY 溶液的 pH7,BX 溶液的 pH7,说明 AY 为强碱弱酸盐,BX 溶液的 pHB若将三种溶液稀释相同倍数,pH 变化最大的是C若分别加入 25 mL 0.1 molL1 盐酸后,pH 最大的是
7、D若三种溶液的 pH 均为 9,则物质的量浓度的大小顺序【答案】C 二、 盐类水解的影响因素1内因弱酸根离子、弱碱阳离子对应的酸、碱越弱,就越易发生水解。如:酸性:CH 3COOHH2CO3 相同浓度的 NaHCO3、CH 3COONa 溶液的 pH 大小关系为 决 定 NaHCO3CH3COONa。2外因因 素 水解平衡 水解程度 水解产生离子的浓度温度 升高 右移 增大 增大增大 右移 减小 增大浓度 减小(即稀释)右移 增大 减小酸 弱碱阳离子水解程度减小外加酸碱碱 弱酸阴离子水解程度减小例如,不同条件对 FeCl3水解平衡的影响Fe 3 3H 2OFe(OH) 33H 条件 移动方向
8、H 数 pH 现象升温 向右 增多 减小 颜色变深通 HCl 向左 增多 减小 颜色变浅加 H2O 向右 增多 增大 颜色变浅加 NaHCO3 向右 减小 增大 生成红褐色沉淀,放出气体命题点 1 外界条件对盐类水解的影响例 7.CH3COONa 水解的离子方程式是 CH3COO H 2OCH 3COOHOH ,当改变下列条件时,将对CH3COONa 水解平衡的影响填入下表:改变条件 移动方向 c(OH ) pH 水解程度升温加 NaOH加水加少量 FeCl3固体加 Na2CO3【答案】改变条件 移动方向 c(OH ) pH 水解程度升温 右移 增大 增大 增大加 NaOH 左移 增大 增大
9、减小加水 右移 减小 减小 增大加少量 FeCl3固体 右移 减小 减小 增大加 Na2CO3 左移 增大 增大 减小命题点 2 水解平衡移动规律的应用例 8漂白粉在溶液中存在下列平衡:ClO H 2OHClO OH ,下列措施能提高其漂白效率的是( )A加 H2O B通入 CO2C通入 SO2 D加少量 NaOH【答案】B 例 9有 4 种混合溶液,分别由等体积 0.1 mol/L 的 2 种溶液混合而成:CH 3COONa 与 Na2CO3;CH 3COONa 与 NaCl; CH 3COONa 与 NaOH;CH 3COONa 与 HCl。c(CH3COO )排序正确的是( )A BC
10、D【答案】A 【解析】、均抑制 CH3COO 水解,但抑制能力更强;中加酸,促进 CH3COO 水解,所以c(CH3COO )排列顺序为。例 10.下图所示三个烧瓶中分别装入含酚酞的 0.01 molL1 CH3COONa 溶液,并分别放置在盛有水的烧杯中,然后向烧杯中加入生石灰,向烧杯中加入 NH4NO3晶体,烧杯中不加任何物质。(1)含酚酞的 0.01 molL1 CH3COONa 溶液显浅红色的原因为_。(2)实验过程中发现烧瓶中溶液红色变深,烧瓶中溶液红色变浅,则下列叙述正确的是_。A水解反应为放热反应B水解反应为吸热反应CNH 4NO3溶于水时放出热量DNH 4NO3溶于水时吸收热量
11、(3)向 0.01 molL1 CH3COONa 溶液中分别加入 NaOH 固体、Na 2CO3固体、FeSO 4固体,使 CH3COO 水解平衡移动的方向分别为_、_、_。(填“左” “右”或“不移动”)。【答案】(1)CH 3COO H 2OCH 3COOHOH ,使溶液显碱性 (2)BD (3)左 左 右三、盐类水解的应用应用一:判断溶液的酸碱性强者显性Na2CO3溶液呈碱性的原因是:CO H 2OHCO OH 23 3应用二:判断盐溶液离子的种类及浓度的大小如 Na2CO3溶液中存在的粒子有:Na 、CO 、H 2CO3、HCO 、OH 、H 、H 2O,且 c(Na )2c(CO )
12、,23 3 23c(OH )c(H )。应用三:判断离子能否共存若阴、阳离子发生水解相互促进的反应,水解程度较大而不能大量共存,有的甚至水解完全。常见的水解相互促进的反应进行完全的有:Fe 3 、Al 3 与 AlO 、CO (HCO )。 2 23 3应用四:判断盐溶液蒸干时所得的产物(1)盐溶液水解生成难挥发性酸和酸根阴离子易水解的强碱盐,蒸干后一般得原物质,如 CuSO4(aq)蒸干得 CuSO4(s);Na 2CO3(aq)蒸干得 Na 2CO3(s)。(2)盐溶液水解生成易挥发性酸时,蒸干灼烧后一般得对应的氧化物,如 AlCl3(aq)蒸干得 Al(OH)3灼烧得 Al2O3。(3)
13、考虑盐受热时是否分解。Ca(HCO 3)2、NaHCO 3、KMnO 4、NH 4Cl 固体受热易分解,因此蒸干灼烧后分别为 Ca(HCO3)2 CaCO 3(CaO);NaHCO 3 Na 2CO3;KMnO 4 K 2MnO4和 MnO2;NH 4Cl NH 3HCl。(4)还原性盐在蒸干时会被 O2氧化如 Na2SO3(aq)蒸干得 Na2SO4(s)。(5)弱酸的铵盐蒸干后无固体。 如 NH4HCO3、(NH 4)2CO3。应用五:保存、配制某些盐溶液如配制 FeCl3溶液时,为防止出现 Fe(OH)3沉淀,常加几滴盐酸来抑制 FeCl3的水解;在实验室盛放Na2CO3、CH 3COO
14、Na、Na 2S 等溶液的试剂瓶不能用玻璃塞,应用橡胶塞。应用六:水解除杂如 MgCl2溶液中混有少量 FeCl3杂质,因 Fe3 的水解程度比 Mg2 水解程度大,可加入 MgO 或 Mg(OH)2或 MgCO3等,使 Fe3 的水解平衡右移,生成 Fe(OH)3沉淀而除去。应用七:利用盐类的水解反应制取胶体、净水如实验室制备 Fe(OH)3胶体的原理为:FeCl 33H 2O Fe(OH)3(胶体)3HCl。= = = = = 明矾净水的原理为:Al 3 水解生成氢氧化铝胶体,胶体具有很大的表面积,吸附水中悬浮物而聚沉。应用八:解释生活、生产中的一些化学现象(1)化肥的施用问题:铵态氮肥与
15、草木灰不得混用,草木灰的主要成分为 K2CO3,当铵态氮肥中的 NH遇到 CO 时,发生相互促进的水解反应,NH 变为 NH3逸出,使氮肥失去效果。 4 23 4(2)泡沫灭火器反应原理:以硫酸铝和小苏打为原料,两种溶液混合后发生相互促进的水解反应,使水解反应趋 于完全,Al 3 3HCO =Al(OH)33CO 2。 3(3)NH4Cl 溶液可作焊接金属的除锈剂:氯化铵溶液呈酸性,能溶解铁锈。(4)热的纯碱水溶液比冷的纯碱水溶液去油污能力强:纯碱溶液中存在 CO 的水解平衡:23CO H 2OHCO OH ,温度升高,水解平衡右移, c(OH )增大,去污能力增强。23 3例 11相同温度、
16、相同浓度的下列六种溶液,其 pH 由小到大的顺序如图所示,图中代表的物质可能分别为( )ANH 4Cl (NH 4)2SO4 CH 3COONaB(NH 4)2SO4 NH 4Cl CH 3COONaC(NH 4)2SO4 NH 4Cl NaOHDCH 3COOH NH 4Cl (NH 4)2SO4【答案】B 【解析】(NH 4)2SO4比 NH4Cl 溶液中的铵根离子浓度大,水解生成的氢离子浓度大,醋酸钠水解显碱性,且其碱性比 Na2CO3要弱。例 12下列指定溶液中一定能大量共存的离子组是( )ApH1 的溶液中:NH 、Na 、Fe 3 、SO 4 24B含有大量 AlO 的溶液中:Na
17、 、K 、HCO 、NO 2 3 3C中性溶液中:K 、Al 3 、Cl 、SO 24DNa 2S 溶液中:SO 、K 、Cu 2 、Cl 24【答案】A 【解析】A 项,酸性条件下,H 抑制 NH 、Fe 3 的水解,能大量共存;B 项, 4AlO HCO H 2O=Al(OH)3CO ,不能大量共存;C 项,Al 3 水解呈酸性,因而在中性溶液中不存 2 3 23在;D 项,Cu 2 S 2 =CuS ,不能大量共存。例 13某校化学实验小组对以下四种物质的水溶液加热蒸干并灼烧,最终不能得到该物质固体的是( )氯化铁 碳酸钠 硫酸亚铁 硅酸钠A仅 B仅C仅 D仅【答案】A 【解析】FeCl
18、 3溶液加热蒸干并灼烧后得到 Fe2O3,碳酸钠溶液在加热蒸干并灼烧后仍为碳酸钠。硫酸亚铁溶液蒸干过程中,被氧化得正三价铁的化合物,硅酸钠溶液蒸干并灼烧后仍为硅酸钠。例 14下列过程或现象与盐类水解无关的是( )A纯碱溶液去油污 B铁在潮湿的环境下生锈C加热氯化铁溶液颜色变深 D浓硫化钠溶液有臭味【答案】B 例 15.下列说法中正确的是( )AAlCl 3溶液和 Al2(SO4)3溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同B配制 FeCl3溶液时,将 FeCl3固体溶解在硫酸中,然后再用水稀释到所需的浓度C向 CuCl2溶液加入 CuO,调节 pH 可除去溶液中混有的 Fe3D泡沫灭


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2019 年高 化学 二轮 复习 专题 16 盐类 水解 溶解 平衡 教案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-58428.html