 四川省乐山市2018年中考化学试题含答案
四川省乐山市2018年中考化学试题含答案
《四川省乐山市2018年中考化学试题含答案》由会员分享,可在线阅读,更多相关《四川省乐山市2018年中考化学试题含答案(8页珍藏版)》请在七七文库上搜索。
1、17将少量下列物质分别放入水中,充分搅拌,不能形成溶液的是( )A蔗糖 B牛奶 C酒精 D白醋18下图所示的家庭小实验中,主要发生物理变化的是( )制取明矾晶体 净水 自制汽水 将鸡蛋壳放入醋中A B C D19 日常生活中,化学无处不在。根据你所掌握的化学知识判断,下列作法中不正确的是( )A用木炭除冰箱异味 B用肥皂水区分硬水和软水C将用过的铁锅洗净擦干以防生锈 D经常将用过的铝锅或铝壶擦拭得光亮如新20乐山是一座亲水城市,水是乐山的灵魂,我们应该象珍惜自己的血液一样珍惜每一滴水。下列关于水的说法中不正确的是( )A水是由氢元素和氧元素组成的化合物 B城市污水应该经过净化处理后再排放C清澈
2、、透明的泉水是纯净物 D水资源是宝贵的,一定要节约用水21下列同学对“SO 2”的认识中,不正确的是A B C D22硅材料是太阳能电池及电脑芯片不可缺少的材料,随着一批多晶硅生产企业在乐山建成投产,乐山将成为我国重要的硅材料产业基地。下面是多晶硅生产过程中的一个重要反应:SiO 2+2C 高 温 Si+2CO,该反应的基本类型是( )A化合反应 B分解反应 C置换反应 D复分解反应23农作物缺磷时,会引起生长迟缓、产量降低,需要施用适量的磷肥。过磷酸钙Ca(H2PO4)2 和 CaSO4 的混合物 是常用的磷肥,其中磷元素的化合价为( )A+2 B+3 C+4 D+524下列各图所示的实验操
3、作,错误的是( )铁丝在 O2 中燃烧 稀释浓硫酸 读取液体体积 称量 NaClA B C D25类推是学习化学的重要方法之一,但盲目类推又可能得出错误结论。下列类推正确的是( )A原子和分子均是微观粒子,原子在化学变化中不能再分,则分子在化学变化中也不能再分B锌和铜均是金属,锌能与稀硫酸反应放出氢气,则铜也能与稀硫酸反应放出氢气C金刚石和石墨均是碳的单质,金刚石十分坚硬,则石墨也十分坚硬DH 2SO4 与 HCl 均是酸,H 2SO4 在水溶液中能电离出 H+,则 HCl 在水溶液中也能电离出 H+26对“大棚”农作物施用“ 汽水 ”(碳酸溶液) ,是近年来在种植生产中兴起的一种新方法。对于
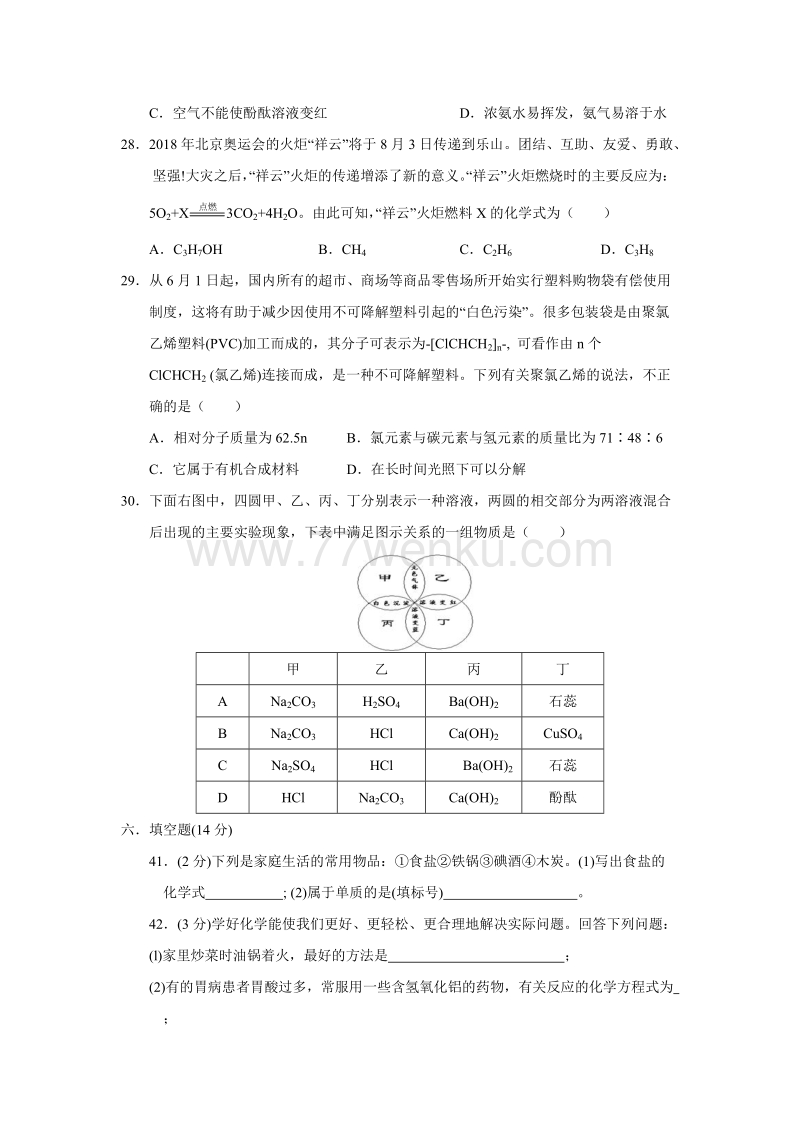
4、其作用的下列几种叙述:加速植物光合作用;冬天有助于农作物“防冻”;有利于改良碱性土壤,调节 pH; 可促进土壤中的 Ca2+、Mg 2+被植物吸收。其中正确的是( )A B C D全部27A、B、C 三只小烧杯内分别依次盛有一定体积的浓氨水、酚酞溶液、酚酞溶液,按下图所示进行探究活动,不能得到的结论是( )A氨水能使酚酞溶液变红 B碱能使酚酞溶液变红C空气不能使酚酞溶液变红 D浓氨水易挥发,氨气易溶于水282018 年北京奥运会的火炬“祥云”将于 8 月 3 日传递到乐山。团结、互助、友爱、勇敢、坚强!大灾之后, “祥云”火炬的传递增添了新的意义。 “祥云”火炬燃烧时的主要反应为:5O2+X
5、点 燃 3CO2+4H2O。由此可知, “祥云”火炬燃料 X 的化学式为( )AC 3H7OH BCH 4 CC 2H6 DC 3H829从 6 月 1 日起,国内所有的超市、商场等商品零售场所开始实行塑料购物袋有偿使用制度,这将有助于减少因使用不可降解塑料引起的“白色污染”。很多包装袋是由聚氯乙烯塑料(PVC)加工而成的,其分子可表示为-ClCHCH 2n-, 可看作由 n 个ClCHCH2 (氯乙烯)连接而成,是一种不可降解塑料。下列有关聚氯乙烯的说法,不正确的是( )A相对分子质量为 62.5n B氯元素与碳元素与氢元素的质量比为 71486C它属于有机合成材料 D在长时间光照下可以分解
6、30下面右图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,下表中满足图示关系的一组物质是( )甲 乙 丙 丁A Na2CO3 H2SO4 Ba(OH)2 石蕊B Na2CO3 HCl Ca(OH)2 CuSO4C Na2SO4 HCl Ba(OH)2 石蕊D HCl Na2CO3 Ca(OH)2 酚酞六填空题(14 分)41(2 分) 下列是家庭生活的常用物品:食盐铁锅 碘酒木炭。(1)写出食盐的化学式 ; (2)属于单质的是(填标号) 。42(3 分) 学好化学能使我们更好、更轻松、更合理地解决实际问题。回答下列问题:(l)家里炒菜时油锅着火,最好的


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 四川省 乐山市 2018 年中 化学试题 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
文档标签
- 化学试题
- 2020乐山
- 四川省乐山市五通桥中学
- 四川省乐山沫若中学
- 四川省泸州市2018年中考化学试题含答案
- 2018年四川省乐山市中考历史试题含答案解析
- 四川省广元市2018年中考化学试题含答案
- 四川省南充市2018年中考化学试题含答案
- 四川省乐山市2018年中考数学试卷含答案解析
- 四川省雅安市2018年中考化学试题含答案解析
- 四川省乐山市2018年中考语文试卷含答案解析版
- 四川省乐山市2018年中考生物试题含答案
- 四川省广元市2018年中考化学试题含答案解析
- 四川省乐山市2018年中考物理试题及答案解析
- 2021年四川省乐山市中考语文试题word版含答案
- 2020年四川省乐山市中考物理试题含答案
- 四川省乐山市2018年中考思想品德试题含答案
- 四川省乐山市2020年中考历史试题含答案
- 四川省乐山市2018年中考物理试题及答案
- 2019年四川省乐山市历史中考试题含答案



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-5352.html