 课题4《化学式与化合价》精品课件
课题4《化学式与化合价》精品课件
《课题4《化学式与化合价》精品课件》由会员分享,可在线阅读,更多相关《课题4《化学式与化合价》精品课件(35页珍藏版)》请在七七文库上搜索。
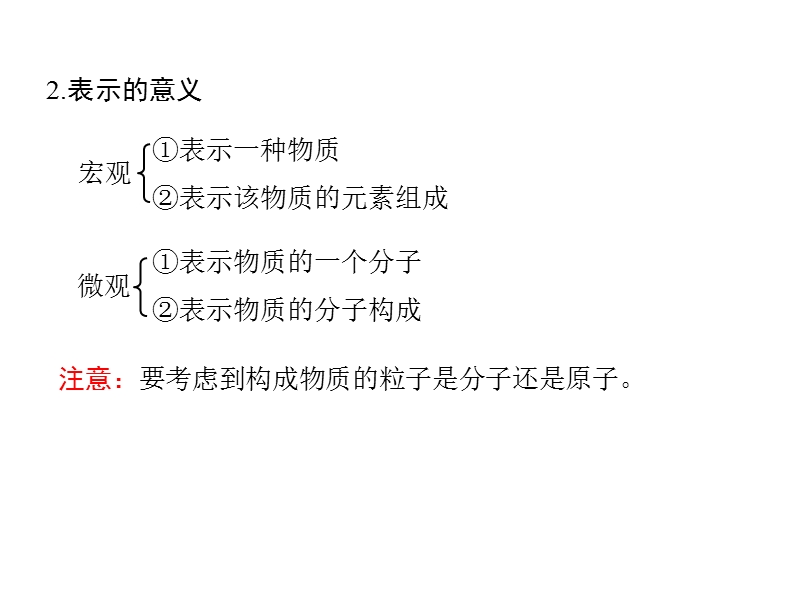
1、,第四单元 自然界的水,课题4 化学式与化合价,1.概念:,注意:每种纯净物的组成是固定不变的,所以,一种物质的化学式只有一个。,如:水 H2O氧气 O2二氧化碳 CO2,用元素符号和数字的组合表示物质组成的式子,叫做化学式。,一、化学式,2.表示的意义,宏观,微观,表示一种物质 表示该物质的元素组成,表示物质的一个分子 表示物质的分子构成,注意:要考虑到构成物质的粒子是分子还是原子。,H2O表示的意义:,表示水这种物质。,表示一个水分子。,表示水由氢元素和氧元素组成。,表示一个水分子由2个氢原子和1个氧原子构成。,宏观意义,微观意义,2 H2O,2个水分子,1个水分子中有2个氢原子,化学式中
2、不同位置的数字表示的意义:,(1)化学式前面的数字表示分子个数。 (2)化学式中元素符号右下角的数字表示每个分子中的原子个数。,化学式中不同位置的数字表示的意义:,(1)由离子构成的物质中不存在一个个的分子,其化学式表示了该物质中各元素原子数目的最简整数比。 (2)一个化学式不一定只表示一种物质,如金刚石和石墨的化学式都是 C,红磷和白磷的化学式都是 P。,特别提醒:,(1)化学式的写法,金属单质: 铁(Fe) 铝(Al) 固态非金属单质:硫(S) 磷(P) 稀有气体: 氖气(Ne) 氦气(He),单质,用元素符号直接 表示化学式,氧气(O2) 氢气(H2) 氮气(N2) 氯气(Cl2),气体
3、非金属单质,在元素符号右下角写上每个分子中所含的原子数目的数字表示化学式,3.化学式的书写和命名,化合物,氧化物:氧元素在后,其他元素在前,同时在相应元素符号的右下角写上每个分子中所含该元素原子数目的数字。 例如:CO2、SO2、H2O等。 其他两种元素形成的化合物:金属元素在前,非金属元素在后,同时在相应元素符号的右下角写上每个分子中所含该元素原子数目的数字。 例如:NaCl、FeCl3等。,原则:顺写反读,一般从右向左读作“某化某”(或“某酸某”),如 NaCl 读作氯化钠,Na2SO4 读作硫酸钠; 有时还需要读出化学式中各种元素的原子的个数,如P2O5 读作五氧化二磷。,(2)化学式的
4、读法,注意:读含有原子团的物质的化学式时,不需读出原子个数。,【例题】豆腐是我国的传统食物。食用豆腐能获得人体所需要的多种氨基酸,其中含量最多的是亮氨酸(化学式:C6H13NO2)。下列有关亮氨酸的说法错误的是( ) A由四种元素组成 B一个分子由 22 个原子构成 C一个亮氨酸分子中含一个氧分子 D属于化合物,C,分析:亮氨酸由碳、氢、氮、氧四种元素组成,A项正确;一个亮氨酸分子中含有6个碳原子、13个氢原子、1个氮原子和2个氧原子,共22个原子,B项正确;亮氨酸属于化合物,由亮氨酸分子构成,不含氧分子,C项错误,D项正确。,1.下列物质的化学式书写不正确的是( ) A.氧化镁 MgO2 B
5、.氧化钠 Na2O C.硫酸锌 ZnSO4 D.氢氧化铜 Cu(OH)2 2.下列化学用语关于数字“3”的意义,说法正确的是( ) 3Hg Fe3+ SO3 3H2O A表示分子个数的是 B表示离子所带电荷数的是 C表示原子个数的是 D表示一个分子中含有某种原子个数的是,A,B,二、化合价,1.化合价的概念 元素的化合价是元素的原子之间形成化合物时表现出来的一种性质,用来表示原子间化合的数目。,例如:在化合物里,O元素通常为-2价,H元素通常为+1价,Cl元素通常为-1价,所以,当氢气与氧气反应时,是 2个氢原子与1个氧原子结合生成 H2O,当氢气与氯气反应时,是 1个氢原子与1个氯原子结合生
6、成 HCl。,作为一个整体参加反应的原子集团(就好像一个原子一样)叫做原子团。原子团也叫做根。,注意:原子团也有化合价,不能单独存在;带电荷的原子团也是离子。例如:,NaOH、 Ca(OH)2 、Cu(NO3)2、NH4NO3、BaSO4、CaCO3、 H3PO4,下列化学式中彩色标记部分为根:,OH: NH4: NO3:,CO32: SO42: PO43:,氢氧根离子,铵根离子,硝酸根离子,碳酸根离子,硫酸根离子,磷酸根离子,2.原子团,3.化合价的有关规律,(1)化合价有正价和负价。 (2)在化合物里氢通常显+1价,氧通常显-2价。 (3)金属元素与非金属元素化合时,金属元素通常显正价,非
7、金属元素通常显负价。 (4)许多元素具有可变化合价,同种元素在不同的化合物里可显不同的化合价,如 FeO、Fe2O3中铁元素的化合价分别为+2和+3;同种元素在同一化合物里也可显示不同的化合价,如 NH4NO3中氮元素的化合价分别为-3和+5。 (5)在任何化合物里,正、负化合价的代数和为零。以H2O为例:( +1 ) 2+(2)=0 (6)单质里元素的化合价为零。,化合价的有关规律:,化合价歌谣,一价氢氯钠钾银, 二价氧钙钡镁锌, 三铝四硅五价磷, 二三铁、二四碳, 二四六硫都齐全, 铜汞二价最常见, 单质零价永不变!,离子符号和化合价的表示方法不同: 离子:数字在前,“+”“-”号在后;写
8、在元素符号或原子团的右上角;数字为1时省略不写。 化合价:数字在后,“+”“-”号在前;写在元素符号或原子团的正上方;数字为1时不能省略。,化合价与离子所带电荷的联系:数字相同,正负号相同。,离子符号与化合价的比较,+1,+2,+3,1,2,4.化合价的书写,(1)根据化学式求某一元素的化合价。,原则:化合物里正、负化合价的代数和为零。,例1:试确定氯酸钾(KClO3)中氯元素的化合价。,解:设氯酸钾中氯元素的化合价为 x,则,(+1)+ x +(2)3=0,解得 x = +5,所以,在氯酸钾中氯元素的化合价为+5。,5.化合价的应用,方法:先将所求元素的化合价设为未知数 x,然后由已知的元素


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 课题 化学式 化合价 精品 课件
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-30261.html