 2018年人教版九年级化学上册期中评估测试卷(含答案解析)
2018年人教版九年级化学上册期中评估测试卷(含答案解析)
《2018年人教版九年级化学上册期中评估测试卷(含答案解析)》由会员分享,可在线阅读,更多相关《2018年人教版九年级化学上册期中评估测试卷(含答案解析)(9页珍藏版)》请在七七文库上搜索。
1、期中评估测试卷(时间:60 分钟 分值:100 分)可能用到的相对原子质量:O16 C12 H1 N14 Cl35.5 Zn65一、选择题(每小题 2分,共 30分)1下列食品、调味品的制作过程中,没有发生化学变化的是( D )解析:水果榨果汁是将水果搅碎、过滤得到汁液,没有生成其他物质,属于物理变化。故选 D。2下列关于空气的说法正确的是( A )A通常情况下,空气中氧气、氮气的体积比为 14B空气中氮气的含量为 78%C空气中二氧化碳的体积只占 0.03%,因此它的作用很小D空气中含量最少的是稀有气体解析:B 项中并未说明是体积分数,故错误;空气中二氧化碳的含量虽然很少,但却是光合作用的主
2、要原料,故 C项错;稀有气体在空气中的含量比二氧化碳多,故 D项错;通常情况下,氧气约占空气总体积的 1/5、氮气约占空气总体积的 4/5,故空气中氧气、氮气的体积比为 14。故选 A。3下列图示实验操作中,正确的是( A )解析:B 中瓶塞没有倒放;C 中试管内液体太多,而且没有用酒精灯外焰加热;D 中称量时物、码位置反了。故选 A。4以下是一些同学在一次实验操作考试中的做法,你认为正确的是( C )A把胶头滴管伸入试管中滴加液体 B在托盘天平上直接称量固体物质C用药匙或纸槽将粉末状药品送入试管底部 D握住试管夹的短柄给试管内的药品加热解析:用滴管滴加液体时,滴管要竖直悬空,A 错误;用托盘
3、天平称量固体物质时,固体物质要放在纸上或玻璃器皿中,B 错误;应握住试管夹的长柄给试管内的药品加热,D 错误。故选 C。5下图是 X、Y 两种元素的原子结构示意图,据图分析,下列判断错误的是( D )AX 是金属元素 BY 元素的原子在化学反应中易得电子CX 和 Y形成化合物的化学式为 MgCl2 DX、Y 两种元素的化学性质很相似解析:X 的原子核内有 12个质子,X 是镁元素,镁是金属元素,A 正确;氯元素的原子最外层有 7个电子,在化学反应中易得到电子形成 8电子稳定结构,故 B正确;镁原子最外层有 2个电子,容易失去,因此镁元素的化合价为2 价,氯原子的最外层有 7个电子,容易得到 1
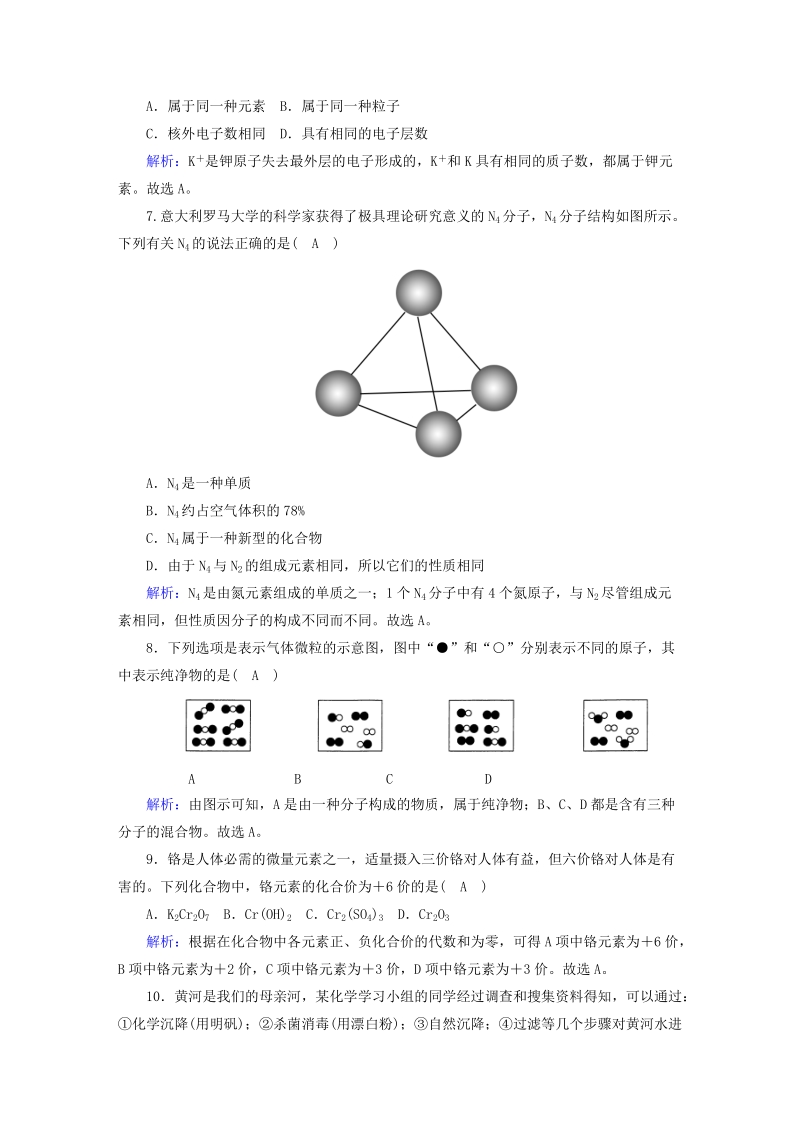
4、个电子,表现为1 价,故 X和 Y形成化合物的化学式为 MgCl2,C 正确;X、Y 两种原子的最外层电子数不同,原子得失电子的能力也不同,因此化学性质不相似,故 D错误。故选 D。6关于 K和 K 的说法,正确的是( A )A属于同一种元素 B属于同一种粒子C核外电子数相同 D具有相同的电子层数解析:K 是钾原子失去最外层的电子形成的,K 和 K具有相同的质子数,都属于钾元素。故选 A。7.意大利罗马大学的科学家获得了极具理论研究意义的 N4分子,N 4分子结构如图所示。下列有关 N4的说法正确的是( A )AN 4是一种单质BN 4约占空气体积的 78%CN 4属于一种新型的化合物D由于
5、N4与 N2的组成元素相同,所以它们的性质相同解析:N 4是由氮元素组成的单质之一;1 个 N4分子中有 4个氮原子,与 N2尽管组成元素相同,但性质因分子的构成不同而不同。故选 A。8下列选项是表示气体微粒的示意图,图中“”和“”分别表示不同的原子,其中表示纯净物的是( A )A B C D解析:由图示可知,A 是由一种分子构成的物质,属于纯净物;B、C、D 都是含有三种分子的混合物。故选 A。9铬是人体必需的微量元素之一,适量摄入三价铬对人体有益,但六价铬对人体是有害的。下列化合物中,铬元素的化合价为6 价的是( A )AK 2Cr2O7 BCr(OH) 2 CCr 2(SO4)3 DCr
6、 2O3解析:根据在化合物中各元素正、负化合价的代数和为零,可得 A项中铬元素为6 价,B项中铬元素为2 价,C 项中铬元素为3 价,D 项中铬元素为3 价。故选 A。10黄河是我们的母亲河,某化学学习小组的同学经过调查和搜集资料得知,可以通过:化学沉降(用明矾);杀菌消毒(用漂白粉);自然沉降;过滤等几个步骤对黄河水进行净化,合理的操作顺序是( B )A B C D解析:净水操作设计原则是:先自然净水,后人工净水;先除去不溶性杂质,后除去可溶性杂质。故选 B。11下列现象或事实,用分子、原子的相关知识加以解释,其中不正确的是( C )现象或事实 解释A 稀有气体可作保护气 原子核外电子达到相
7、对稳定结构B 氧气和臭氧(O 3)性质不完全相同 构成物质的分子不同C 物质热胀冷缩 分子大小随温度改变而改变D 水通电分解 在化学变化中分子可以再分解析:物质具有热胀冷缩的性质,原因是构成物质的分子间间隔会随温度的改变而变化,但分子的大小不会发生改变。由此,C 错误。故选 C。12很多饮料中都含有柠檬酸(C 6H8O7)。下列关于柠檬酸的说法中正确的是( C )A属于氧化物 B由 6个碳原子、8 个氢原子和 7个氧原子组成C氧元素的质量分数最大 D碳、氢、氧三种元素的质量比为 687解析:柠檬酸中有 C、H、O 三种元素,不属于氧化物,故 A错误;柠檬酸由 C、H、O 三种元素组成,每个柠檬
8、酸分子由 6 个碳原子、8 个氢原子和 7个氧原子构成,故 B错误;由柠檬酸分子的构成,及各原子的相对原子质量可推知,氧元素的质量分数最大,故 C正确;柠檬酸中 C、H、O 三种元素的质量比(126)(18)(167)9114,故 D错误。故选 C。13世界卫生组织将某氧化物 RO2列为 A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛应用。实验测得该氧化物中 R与 O的质量比为 7164,则 RO2的化学式为( B )ACO 2 BClO 2 CSO 2 DNO 2解析:设 R原子的相对原子质量为 x,则有: ,x162 7164x 16235.5,所以,R 元素为氯元素。故选
9、 B。716414下列含氯物质的化学式中,氯元素的化合价最低的是( C )A用于漂白杀菌的次氯酸钠(NaClO) B用作鱼塘的杀菌消毒剂(ClO 2)C用来调味的食盐(NaCl) D氯酸钾(KClO 3)解析:根据化合物中各元素正、负化合价的代数和为 0的原则可知:次氯酸钠中氯元素的化合价为1,二氧化氯中氯元素的化合价为4,食盐中氯元素的化合价为1,氯酸钾中氯元素的化合价为5。故选 C。15有关尿素CO(NH 2)2的说法正确的是( C )A尿素的相对分子质量为 12161412246B尿素是一种氧化物C尿素中碳、氧、氮、氢四种元素的质量比为 3471D尿素中氮元素质量分数的计算式为 100%


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-26786.html