 2018-2019学年鲁科版高中化学选修3:第2节第2课时核外电子排布与元素周期表学案(含答案)
2018-2019学年鲁科版高中化学选修3:第2节第2课时核外电子排布与元素周期表学案(含答案)
《2018-2019学年鲁科版高中化学选修3:第2节第2课时核外电子排布与元素周期表学案(含答案)》由会员分享,可在线阅读,更多相关《2018-2019学年鲁科版高中化学选修3:第2节第2课时核外电子排布与元素周期表学案(含答案)(7页珍藏版)》请在七七文库上搜索。
1、第 2 课时 核外电子排布与元素周期表、原子半径1.了解核外电子的排布规律与元素周期表中周期、族划分的关系,并能解释它们之间的变化规律。 (重点)2.了解原子半径的具体意义及其测定方法,并能够解释原子半径的周期性变化规律。(难点)3.了解元素周期表的应用价值。核外电子排布与元素周期表基础初探教材整理 1 核外电子排布与周期的划分1.周期与能级组、原子轨道的对应关系2.原子核外电子排布与元素周期表中周期划分的本质联系7个 能 级 组 分 别 对 应 7个 周 期能 级 组 最 多 容 纳 电 子 数 等 于 本 周 期 所 包 含 元 素 的 种 数3周期数与电子层数的关系周期数最外层电子所在轨
2、道的主量子数。(1)周期序数电子层数对应能级组数。()(2)同一能级组内能级之间的能量差较小,而相邻能级组之间的能量差较大。()(3)原子的最外层电子排布为 3d14s2,该元素位于第四周期。()教材整理 2 核外电子排布与族的划分1划分依据取决于原子的价电子数目和价电子排布。2特点同族元素的价电子数目和价电子排布相同。3规律(1) (2) (3)稀有气体价电子排布: ns2np6(He 除外)。(1)主族元素的价电子数全部排布在最外层的 ns 轨道上。()(2)主族序数该元素原子价电子数。()(3)同一副族不同元素原子价电子排布完全相同。()(4)0 族元素很稳定,化合价常为 0,故其价电子
3、也为 0。()合作探究探究背景不同元素在周期表中有固定的位置,而且每一周期所包含元素种类可能不同。探究问题1如何确定主族元素在周期表中的位置?【提示】 首先由元素的原子序数,写出该元素原子结构的电子排布式或价电子排布式,再依据下列方法确定周期序数和族序数。(1)元素原子的电子层数周期数。(2)主族元素原子的价电子数该元素在周期表中的族序数。2同属长周期的 4、5、6 周期所包含的元素种类数分别为 18、18、32,并解释其原因。【提示】 18、18、32。据鲍林近似能级图,第 4、5 周期元素包含的能级为 ns、 np、( n1)d,共有 9 个原子轨道,最多容纳 18 个电子,对应两周期中各
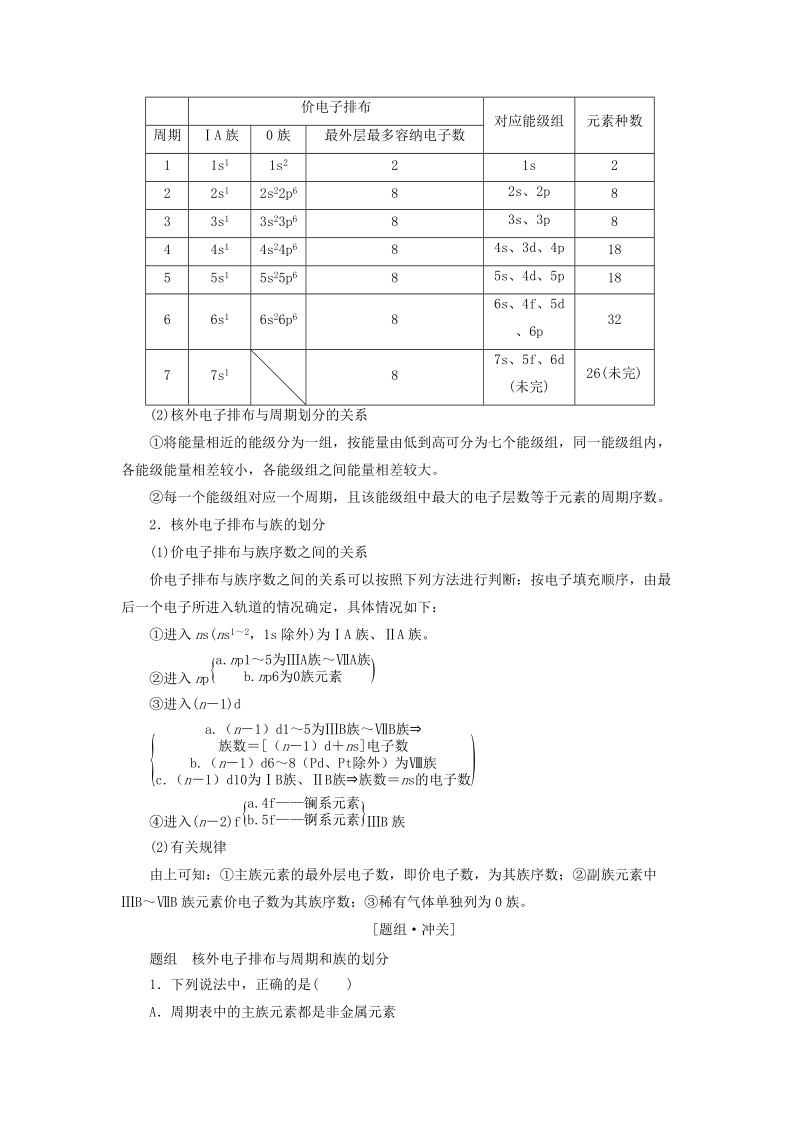
4、 18 种元素;而第 6 周期元素能级除 ns、 np 和(n1)d 外,还有( n2)f,故多出 7 个原子轨道即 14 个电子,对应多出 14 种元素。核心突破1核外电子排布与周期的划分(1)每一周期元素原子的价电子排布和元素种数的关系价电子排布周期 A 族 0 族 最外层最多容纳电子数对应能级组 元素种数1 1s1 1s2 2 1s 22 2s1 2s22p6 8 2s、2p 83 3s1 3s23p6 8 3s、3p 84 4s1 4s24p6 8 4s、3d、4p 185 5s1 5s25p6 8 5s、4d、5p 186 6s1 6s26p6 86s、4f、5d、6p 327 7s
5、1 87s、5f、6d(未完)26(未完)(2)核外电子排布与周期划分的关系将能量相近的能级分为一组,按能量由低到高可分为七个能级组,同一能级组内,各能级能量相差较小,各能级组之间能量相差较大。每一个能级组对应一个周期,且该能级组中最大的电子层数等于元素的周期序数。2核外电子排布与族的划分(1)价电子排布与族序数之间的关系价电子排布与族序数之间的关系可以按照下列方法进行判断:按电子填充顺序,由最后一个电子所进入轨道的情况确定,具体情况如下:进入 ns(ns12 ,1s 除外)为A 族、A 族。进入 npa.np1 5为 A族 A族b.np6为 0族 元 素 )进入( n1)da.( n 1)
6、d1 5为 B族 B族 族 数 ( n 1) d ns电 子 数b.( n 1) d6 8( Pd、 Pt除 外 ) 为 族c.( n 1) d10为 B族 、 B族 族 数 ns的 电 子 数 )进入( n2)f B 族a.4f镧 系 元 素b.5f锕 系 元 素 (2)有关规律由上可知:主族元素的最外层电子数,即价电子数,为其族序数;副族元素中BB 族元素价电子数为其族序数;稀有气体单独列为 0 族。题组冲关题 组 核 外 电 子 排 布 与 周 期 和 族 的 划 分1下列说法中,正确的是( )A周期表中的主族元素都是非金属元素B周期表中的主族元素都是金属元素C周期表中的非金属元素都位于
7、短周期D周期表中的过渡元素都是金属元素【解析】 第A 族都是金属元素,A 错;第A 族元素都是非金属元素,B 错;A、A、A 族的非金属元素,长、短周期都有,C 错;D 符合题意。【答案】 D2在元素周期表中,原子最外电子层只有 2 个电子的元素是( )A一定是金属元素 B一定是稀有气体元素C一定是过渡元素 D无法判断是哪一类元素【解析】 原子最外电子层只有 2 个电子的元素如 He、Mg、Fe 等,看来无法判断是哪一类元素。【答案】 D3价电子排布为 5s25p1的元素,在周期表中的位置是( )A第 4 周期第A 族 B第 5 周期第A 族C第 5 周期第A 族 D第 4 周期第A 族【解析


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2018 2019 学年 鲁科版 高中化学 选修 课时 核外电子 排布 元素 周期表 学案含 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-25076.html