 2023年上海市松江区中考一模化学试卷(含答案解析)
2023年上海市松江区中考一模化学试卷(含答案解析)
《2023年上海市松江区中考一模化学试卷(含答案解析)》由会员分享,可在线阅读,更多相关《2023年上海市松江区中考一模化学试卷(含答案解析)(18页珍藏版)》请在七七文库上搜索。
1、2023年上海市松江区中考一模化学试题相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 K-39 Ca-40 Mn-55一、选择题(1-44每题均只有一个正确选项,15-77每题均有12个正确选项)1. 属于化学性质的是()A. 沸点B. 熔点C. 可燃性D. 密度2. 会造成酸雨的物质是A. SO2B. COC. O2D. N23. 生活中的白醋呈酸性,室温时,白醋的pH可能为A. 3B. 7C. 10D. 134. 在水净化过程中,属于化学变化的是A. 挥发B. 过滤C. 消毒D. 吸附5. 与金刚石互为同素异形体的是A. 木炭B. 石墨C. 一氧化碳D. 二氧化碳6.
2、对食品中各种“剂”的物质描述错误的是A. 食盐作调味剂B. 生石灰作干燥剂C. 干冰作制冷剂D. 氧气作防腐剂7. 工业上常把煤块粉碎后使其充分燃烧,其目的是A. 减少氧气的消耗B. 提高煤的利用率C. 减少二氧化碳的排放D. 减少酸雨的形成8. 实验室制取二氧化碳,能随开随用、随关随停实验装置是A. B. C. D. 9. 关于1mol过氧化氢(H2O2)说法正确的是A. 含1mol氧分子B. 摩尔质量为34克C. 氢氧元素的质量比为1:1D. 含氢元素2克10. 能表示如图细口瓶中水的“量”最适合的是A. 1000g水分子B. 100克水C 6.021023mol水D. 1000毫升水11
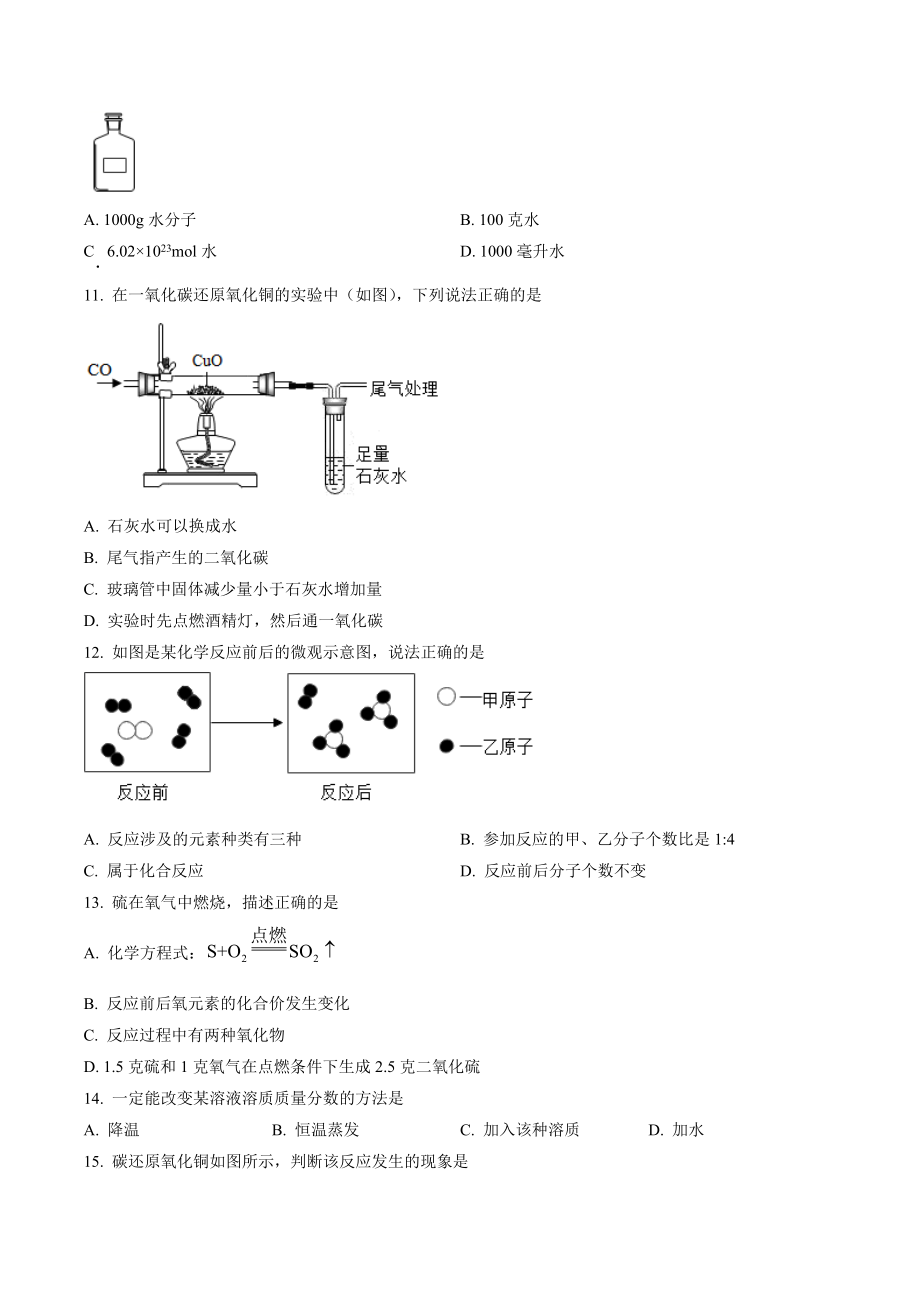
3、. 在一氧化碳还原氧化铜的实验中(如图),下列说法正确的是A. 石灰水可以换成水B. 尾气指产生的二氧化碳C. 玻璃管中固体减少量小于石灰水增加量D. 实验时先点燃酒精灯,然后通一氧化碳12. 如图是某化学反应前后的微观示意图,说法正确的是A. 反应涉及的元素种类有三种B. 参加反应的甲、乙分子个数比是1:4C. 属于化合反应D. 反应前后分子个数不变13. 硫在氧气中燃烧,描述正确的是A. 化学方程式:B. 反应前后氧元素的化合价发生变化C. 反应过程中有两种氧化物D. 1.5克硫和1克氧气在点燃条件下生成2.5克二氧化硫14. 一定能改变某溶液溶质质量分数的方法是A. 降温B. 恒温蒸发C
4、. 加入该种溶质D. 加水15. 碳还原氧化铜如图所示,判断该反应发生的现象是A. 被加热试管的管口有无色液滴B. 生成无色气体C. 导管口冒气泡D 固体由黑色变红色16. 天气瓶是有趣的装饰品,瓶中物质M在不同的天气会产生不同的晶体变化,现象如图。下列描述正确的是A. 天气瓶中物质是纯净物B. 物质M的溶解度随压强的减小而减小C. 物质M的溶解度随温度降低而减小D. 从晴天到下雪天的过程中,物质M溶质质量分数依次减小17. 取24.5克氯酸钾和一定量二氧化锰混合,加热,收集一瓶氧气后停止实验,测得剩余固体的质量为m克。下列分析正确的是A. 生成氧气质量是(24.5-m)克B. 生成氯化钾质量
5、小于m克C. 二氧化锰质量可能是8.7克D. m可能是14.9二、简答题18. 人类生活在空气中,空气与人类的生存休戚相关。(1)空气中最多的气体是_,空气是_(选填“纯净物”或“混合物”)。(2)自然界中既有消耗氧气又有产生氧气变化,使空气中氧气的含量基本保持不变,为人类的生存提供保证。请分别写出你学过的一个消耗氧气和一个产生氧气的化学方程式_;_。(3)空气质量对人体健康有直接影响。雷电时,空气中产生少量臭氧气体,臭氧具有杀菌消毒的作用。臭氧的化学式为O3,氧元素的存在形态是_(选填“游离态”或“化合态”),1mol臭氧分子的个数约为_个。(4)我国承诺将力争2030年前实现“碳达峰”,在
6、2060年前实现“碳中和”。其中“碳”代表的物质是_。19. 实验室制取气体是化学学习的重要内容。(1)大理石和稀盐酸制取二氧化碳的化学方程式是_;收集二氧化碳的方法是_,将点燃的木条伸入盛有二氧化碳的集气瓶中,现象是_,由此_(选填“能”或“不能”)判断集气瓶中集满二氧化碳。(2)按下表进行实验,分别取等质量的大理石加入足量稀盐酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如下图所示:实验编号药品I块状大理石、10%HCl溶液II大理石粉末、10%HCl溶液两次实验中参与反应的盐酸质量是_(选填“相等”或“不相等”)。曲线乙对应实验_(选填“I”或“II”),你的判断依据是_。若用曲
7、线甲对应的药品进行制取二氧化碳实验,合适的发生装置是_。(填编号)20. 依据硝酸钾和氯化钠的溶解度曲线,回答问题。(1)氯化钠属于_(选填“易溶物”或“难溶物”)。(2)60时,把接近饱和的氯化钠溶液变成饱和溶液的方法是_。(3)60时,100克硝酸钾饱和溶液的溶质质量分数为_(列式即可),倒出部分该溶液,从“量”的角度对比剩余溶液和原溶液。剩余溶液中的溶质质量比原溶液中溶质质量_(选填“大”“小”或“相等”);剩余溶液中的_与原溶液相同。(4)某溶液中含有硝酸钾和氯化钠,对该溶液进行如下操作:操作X的名称是_(选填“蒸发结晶”或“降温结晶”)。有关说法正确的是_。A.滤渣一定含硝酸钾B.滤
8、渣一定含氯化钠C.原溶液是硝酸钾的饱和溶液D.滤液甲和滤液乙中都含有两种溶质21. 煅烧10克碳酸钙并检验相关成分,根据实验过程填空。(1)操作的名称是_。往滤液中滴加无色酚酞,现象是_。(2)碳酸钙煅烧分解的化学方程式是_,灼烧后的固体中氧化钙是_克。(3)10克碳酸钙有a克钙元素,7.8克固体中含有b克钙元素,滤渣中含有c克钙元素。则a、b、c的大小关系是:_,并说明判断依据_。(4)为确定滤渣的成分,还需要的一个信息是_。2023年上海市松江区中考一模化学试题相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 K-39 Ca-40 Mn-55一、选择题(1-44每题均只有
9、一个正确选项,15-77每题均有12个正确选项)1. 属于化学性质是()A. 沸点B. 熔点C. 可燃性D. 密度【答案】C【解析】【分析】物质通过化学变化表现出来的性质就是物质的化学性质,不需要通过化学变化表现出来的性质是物理性质。【详解】A、物质的沸点属于物理性质,A选项错误,不符合题意;B、物质的熔点属于物理性质,B选项错误,不符合题意;C、物质的可燃性属于化学性质,C选项正确,符合题意;D、物质的密度属于物理性质,D选项错误,不符合题意。故选C。2. 会造成酸雨的物质是A. SO2B. COC. O2D. N2【答案】A【解析】【详解】煤燃烧时排放出的二氧化硫、二氧化氮等污染物,这些气
10、体或气体在空气中发生反应后的生成物溶于雨水,会形成酸雨,故选A。3. 生活中的白醋呈酸性,室温时,白醋的pH可能为A. 3B. 7C. 10D. 13【答案】A【解析】【详解】生活中的白醋呈酸性,pH7,故室温时,白醋的pH可能为3。故选A。4. 在水的净化过程中,属于化学变化的是A. 挥发B. 过滤C. 消毒D. 吸附【答案】C【解析】【详解】A、挥发的过程是水由液态变为气态,是状态的改变,没有新物质生成,属于物理变化,不符合题意;B、过滤的过程中只是将不溶物与水分离,没有新物质生成,属于物理变化,不符合题意;C、消毒的过程中消毒剂能破坏细菌中的物质,从而使细菌失去活性,杀菌消毒的过程中有新
11、物质生成,属于化学变化,符合题意;D、吸附是利用了活性炭的吸附性,没有新物质生成,属于物理变化,不符合题意,故选C5. 与金刚石互为同素异形体的是A. 木炭B. 石墨C. 一氧化碳D. 二氧化碳【答案】B【解析】【分析】同素异形体是指由同种元素组成的不同单质,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质。【详解】A、木炭的主要成分是碳,属于混合物,与金刚石不属于同素异形体,故选项错误。B、石墨和金刚石均是碳元素形成的不同单质,互为同素异形体,故选项正确。C、一氧化碳是化合物,与金刚石不属于同素异形体,故选项错误。D、二氧化碳是化合物,与金刚石不属于同素异形体,故选项错误。故选
12、:B。6. 对食品中各种“剂”的物质描述错误的是A. 食盐作调味剂B. 生石灰作干燥剂C. 干冰作制冷剂D. 氧气作防腐剂【答案】D【解析】【详解】A、氯化钠是重要的调味品,食盐的主要成分是氯化钠,所以食盐作调味剂。A正确;B、生石灰与水反应生成氢氧化钙,所以生石灰作干燥剂吸收某些物质中的水分。B正确;C、固态二氧化碳叫干冰,干冰升华制冷,所以干冰作制冷剂。C正确;D、氧气具有氧化性,是氧化剂,不能用作防腐剂。D错误。综上所述:选择D。7. 工业上常把煤块粉碎后使其充分燃烧,其目的是A. 减少氧气的消耗B. 提高煤的利用率C. 减少二氧化碳的排放D. 减少酸雨的形成【答案】B【解析】【详解】工
13、业上常把煤块粉碎,其目的是增大煤和氧气的接触面积,使其充分燃烧提高煤的利用率。故选B。8. 实验室制取二氧化碳,能随开随用、随关随停的实验装置是A. B. C. D. 【答案】C【解析】【详解】A.关闭止水夹,不能使固体和液体分离,不能随开随用、随关随停,错误;B.长颈漏斗伸入试管内的长度太短,关闭止水夹,液体无法倒流回长颈漏斗不能使固体和液体分离,不能随开随用、随关随停,错误;C. 关闭止水夹,液体倒流回长颈漏斗,能使固体和液体分离,能随开随用、随关随停,正确;D. 关闭止水夹,不能使固体和液体分离,不能随开随用、随关随停,错误。故选C。9. 关于1mol过氧化氢(H2O2)说法正确的是A.
14、 含1mol氧分子B. 摩尔质量为34克C. 氢氧元素的质量比为1:1D. 含氢元素2克【答案】D【解析】【详解】A、过氧化氢是由过氧化氢分子构成,其中不含有氧分子,错误;B、摩尔质量的单位为g/mol,错误;C、过氧化氢中氢、氧元素的质量比=(12):(162)1:1,错误;D、1mol过氧化氢含氢元素质量=34g/mol1mol=2g,正确。故选D。10. 能表示如图细口瓶中水的“量”最适合的是A. 1000g水分子B. 100克水C. 6.021023mol水D. 1000毫升水【答案】D【解析】【详解】A、水分子是微观概念,不能体现在细口瓶上,故A不符合题意;B、水的质量需要通过计算得
15、出,不能直观体现在细口瓶上,故B不符合题意;C、摩尔是微观概念,不能体现在细口瓶上,故C不符合题意;D、液体用量筒量取,则体积可以表示细口瓶中水的量,故D符合题意;故选D。11. 在一氧化碳还原氧化铜的实验中(如图),下列说法正确的是A. 石灰水可以换成水B. 尾气指产生的二氧化碳C. 玻璃管中固体减少量小于石灰水增加量D. 实验时先点燃酒精灯,然后通一氧化碳【答案】C【解析】【详解】A、石灰水验证是否生成二氧化碳,不能换成水,因为二氧化碳溶解于水,无明显现象,故A错误;B、尾气是指一氧化碳,一氧化碳有毒,会污染空气,二氧化碳不会污染空气,故B错误;C、一氧化碳还原氧化铜生成铜和二氧化碳,玻璃
16、管中固体减少的是反应的氧化铜中氧元素的质量,石灰水吸收二氧化碳,增加量是生成的二氧化碳的质量,根据化学方程式,玻璃管中固体减少量小于石灰水增加量,故C正确;D、实验时先通一氧化碳,排尽装置内空气,防止爆炸,然后点燃酒精灯,故D错误。故选C。12. 如图是某化学反应前后的微观示意图,说法正确的是A. 反应涉及的元素种类有三种B. 参加反应的甲、乙分子个数比是1:4C. 属于化合反应D. 反应前后分子个数不变【答案】C【解析】【分析】由化学反应前后的微观示意图可知,在反应过程中有1个“”粒子没有参加反应,各物质反应的微粒数目关系是: 。【详解】A、根据微观示意图可知,反应中涉及两种原子,即涉及元素


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2023 上海市 松江区 中考 化学 试卷 答案 解析
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-237594.html