 第四单元自然界的水 单元测试题(含答案)2022-2023学年人教版九年级化学上册
第四单元自然界的水 单元测试题(含答案)2022-2023学年人教版九年级化学上册
《第四单元自然界的水 单元测试题(含答案)2022-2023学年人教版九年级化学上册》由会员分享,可在线阅读,更多相关《第四单元自然界的水 单元测试题(含答案)2022-2023学年人教版九年级化学上册(8页珍藏版)》请在七七文库上搜索。
1、第四单元自然界的水第四单元自然界的水 一、单选题一、单选题 1关于水的说法错误的是 A海洋是一个巨大的资源宝库,含有丰富的水资源和化学资源 B水体污染的来源主要有工业污染、农业污染和生活污染 C自来水厂净水过程中既含有化学变化又含有物理变化 D市场上出售的瓶装纯净水是纯净物 2下列实验现象或操作描述正确的是 A红磷在氧气中燃烧,产生大量的白雾 B用酒精灯加热试管里的液体时,试管口不要对着自己或他人 C过滤液体时,将烧杯中的液体直接倾倒入漏斗中 D氢气在空气中燃烧时,产生黄色火焰 3“南水北调”工程是我国的一项重大战略性基础设施,功在当代,利在千秋,为切实从守护生命线的政治高度对它加以维护,我们
2、要努力做到 A扩大沿线工业生产 B采集沿线各种排水 C保障水质清洁安全 D加大沿途矿产开采 4甘草酸苷(化学式为 C42H61O16NH4)是中药甘草的一种成分,具有解毒作用,其相对分子质量为 839,熔点为 212,关于它的表述正确的一项是 A属于混合物 B由四种元素组成 C常温下呈液态 D质量为 839g 5替诺福韦(化学式为 C9H14N5O4P)是一种抗病毒药物,在 5565的环境中反应制成,其相对分子质量为 287.22。下列关于它的表述正确的一项是 A受热即可分解 B属于混合物 C质量为 287.22g D由五种元素组成 6由太湖水生产自来水的部分处理过程如下。有关说法不正确的是
3、A用细沙“过滤”可滤除水中的细小颗粒 B用活性炭“吸附”可除去水中的色素和异味 C上述处理过程应包含“蒸馏” D经过处理获得的自来水仍是混合物 7铷(Rb)原子钟被称作北斗卫星的“心脏”、下图为铷原子的结构示意图,下列说法不正确的是 A铷原子核内的质子数为 37 B铷原子在化学变化中容易失去 1 个电子 C铷原子的核外电子分 5 层排布 D氯化铷的化学式为 RbCl2 8广州北部水厂采用了先进的超滤膜净水技术,超滤膜能有效去除水中的悬浮物、藻类、细菌等不溶性杂质。关于水的净化,下列说法不正确的是 A加入明矾能促进水中悬浮杂质沉降 B活性炭可除去水中异味 C超滤膜可降低水的硬度 D自来水属于混合
4、物 9“酒是陈的香”。酒的主要成分为乙醇,在 525的温度下存储,酒的香味可以变得更浓郁。原因是少量乙醇被氧化成乙酸(有刺激性气味) ,乙酸与乙醇反应生成了乙酸乙酯(化学式为 CH3COOC2H5) 。下列关于乙酸乙酯的说法中不正确的是 A乙酸乙酯具有香味 B乙酸乙酯属于有机物 C乙酸乙酯中氧、氢元素的质量比为 4:1 D乙酸乙酯是由 4 个碳原子、8 个氢原子和 2 个氧原子构成的 10化学符号具有独特的学科内涵。下列各项对相关符号含义的说法正确的是 A2H2O2:只能表示 2 个过氧化氢分子 B2-3SO:只能表示硫酸根离子 C只能表示氩原子的结构示意图: DAg:只能表示金属银 11疫情
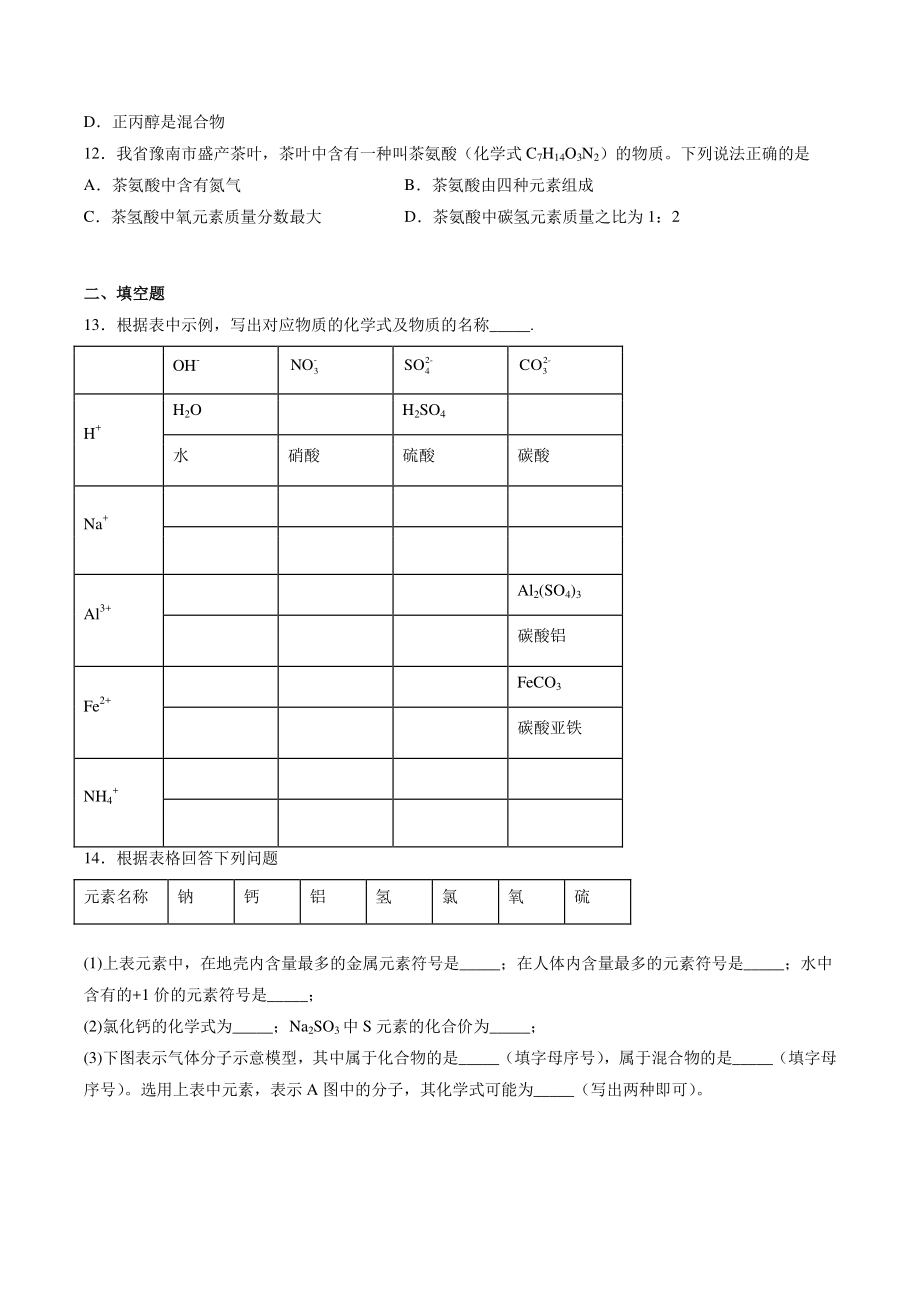
5、防控期间用到一种免洗手消毒凝胶,其中含有正丙醇(C3H8O) 。下列有关正丙醇的说法正确的是 A正丙醇相对分子质量为 60g B碳元素的质量分数是 60% C碳、氢元素的质量比为 3:8 D正丙醇是混合物 12我省豫南市盛产茶叶,茶叶中含有一种叫茶氨酸(化学式 C7H14O3N2)的物质。下列说法正确的是 A茶氨酸中含有氮气 B茶氨酸由四种元素组成 C茶氢酸中氧元素质量分数最大 D茶氨酸中碳氢元素质量之比为 1:2 二、填空题二、填空题 13根据表中示例,写出对应物质的化学式及物质的名称_. OH- -3NO 2-4SO 2-3CO H+ H2O H2SO4 水 硝酸 硫酸 碳酸 Na+ Al
6、3+ Al2(SO4)3 碳酸铝 Fe2+ FeCO3 碳酸亚铁 NH4+ 14根据表格回答下列问题 元素名称 钠 钙 铝 氢 氯 氧 硫 (1)上表元素中,在地壳内含量最多的金属元素符号是_;在人体内含量最多的元素符号是_;水中含有的+1 价的元素符号是_; (2)氯化钙的化学式为_;Na2SO3中 S 元素的化合价为_; (3)下图表示气体分子示意模型,其中属于化合物的是_(填字母序号) ,属于混合物的是_(填字母序号) 。选用上表中元素,表示 A 图中的分子,其化学式可能为_(写出两种即可) 。 15化学从宏观和微观两个角度认识物质。图甲是两种元素在元素周期表中的信息,图乙是钠原子和氧原
7、子的原子结构示意图。 (1)图甲的横线上填的是_,图乙横线上的数字是_。 (2)根据图乙的信息,写出氧化钠的化学式_。 16水被誉为“生命之源”,在生产、生活中有重要的作用。 (1)如图 1 是电解水的装置示意图,其中发生反应的文字表达式为_。在实验过程中,试管 a 中收集到的气体是_。 (2)电解水实验揭示了水是由_组成的。 (3)自来水生产的简要流程可用如图 2 表示: 能除去水中的固体杂质的是_(填“过滤池”或“吸附池”) ; 吸附池通常加有活性炭,其作用是_; 输送到用户家中的自来水_(填“是”或“不是”)纯净物。请用简单的方法证明你的判断:_。 17书写物质的化学式: A单质化学式的


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第四单元自然界的水 单元测试题含答案2022-2023学年人教版九年级化学上册 第四 单元 自然界 单元测试 答案 2022 2023 学年 人教版 九年级 化学 上册
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-220756.html