 第二节 氯及其化合物(第3课时)氯气的制备 作业练习(含答案)
第二节 氯及其化合物(第3课时)氯气的制备 作业练习(含答案)
《第二节 氯及其化合物(第3课时)氯气的制备 作业练习(含答案)》由会员分享,可在线阅读,更多相关《第二节 氯及其化合物(第3课时)氯气的制备 作业练习(含答案)(13页珍藏版)》请在七七文库上搜索。
1、第二章 海水中的重要元素钠和氯 第第二二节节 氯氯及其化合物及其化合物 第第 3 课时课时 氯气的制备氯气的制备 一、选择题一、选择题 1 (2019 福建省尤溪第一中学高一月考)下列关于氯及其化合物的叙述正确的是( ) A氯气的性质很活泼,它与氢气混合后立即发生爆炸 B实验室制取氯气时,为了防止环境污染,多余的氯气可以用饱和食盐水吸收 C久置的氯水没有漂白性 D检验 HCl 气体中是否混有 2 Cl的方法是将气体通入硝酸银溶液 2下列离子方程式的书写正确的是( ) A实验室用大理石和稀盐酸制取 CO2:2H+CO32-=CO2+H2O B钠与水反应:Na+2H2O=Na+2OH-+H2 C将
2、稀硫酸滴在铜片上: Cu+2H+=Cu2+H2 D有效成分为NaClO的消毒液与有效成分为浓HCl的洁厕灵混用产生黄绿色气体: 22 ClOCl2H =ClH O 3 (2020 衡东县欧阳遇实验中学高一期末)下列除去杂质的实验方法正确的是 A除去 Cl2中的少量 HCl:通过饱和 NaHCO3溶液,收集气体 B除去 K2CO3固体中少量 NaHCO3:置于坩埚中加热 C除去 KCl溶液中的少量 MgCl2:加入适量 NaOH溶液,过滤 D除去氢氧化铁胶体中的 Cl:渗析 4 (2020 云南省高一期末)实验室用浓盐酸和二氧化锰制氯气。下列说法错误的是 A浓盐酸在该反应中表现出酸性和还原性 B
3、该方法是瑞典化学家舍勒最先发现的 C该反应的氧化产物是二氯化锰,还原产物是氯气 D该反应的离子方程式为 MnO2+4H+2Cl- Mn2+Cl2+2H2O 5 (2020 营口市第二高级中学高一期末)实验室里可按下图所示的装置来干燥、收集气体 R,多余的气体 R可用水吸收,则 R 是 AHCl BCl2 CCO DNH3 6 (2020 阜新市第二高级中学高一期末)下列装置应用于实验室制取氯气并回收氯化锰溶液,不能达到实 验目的的是 A用装置甲制取氯气 B用装置乙除去氯气中的少量氯化氢 C用装置丙收集氯气并防止污染空气 D用装置丁分离二氧化锰和氯化锰溶液 7(2020 内蒙古科左后旗甘旗卡第二
4、高级中学高一期末) 实验室用下列两种方法制取氯气: 用含 292g HCl 的浓盐酸与足量的 MnO2反应;用 174g MnO2与足量浓盐酸反应。若不考虑 HCl的挥发,则反应后所得 氯气的质量( ) A方法比方法多 B方法比方法多 C两种方法一样多 D无法比较 8人类的生产生活离不开化学,下列关于生活中的化学知识说法错误的是( ) A用浓盐酸与漂粉精反应能制得氯气 B可用碳酸氢钠治疗胃酸过多 C二氧化碳是形成酸雨的主要原因 D不需要通过化学反应就能从海水中获得食盐和淡水 9 (2020 浙江省高二期末改编)下列说法不正确 的是 A将氯气通入紫色石蕊溶液中,可以看到石蕊溶液先变红后褪色 B用
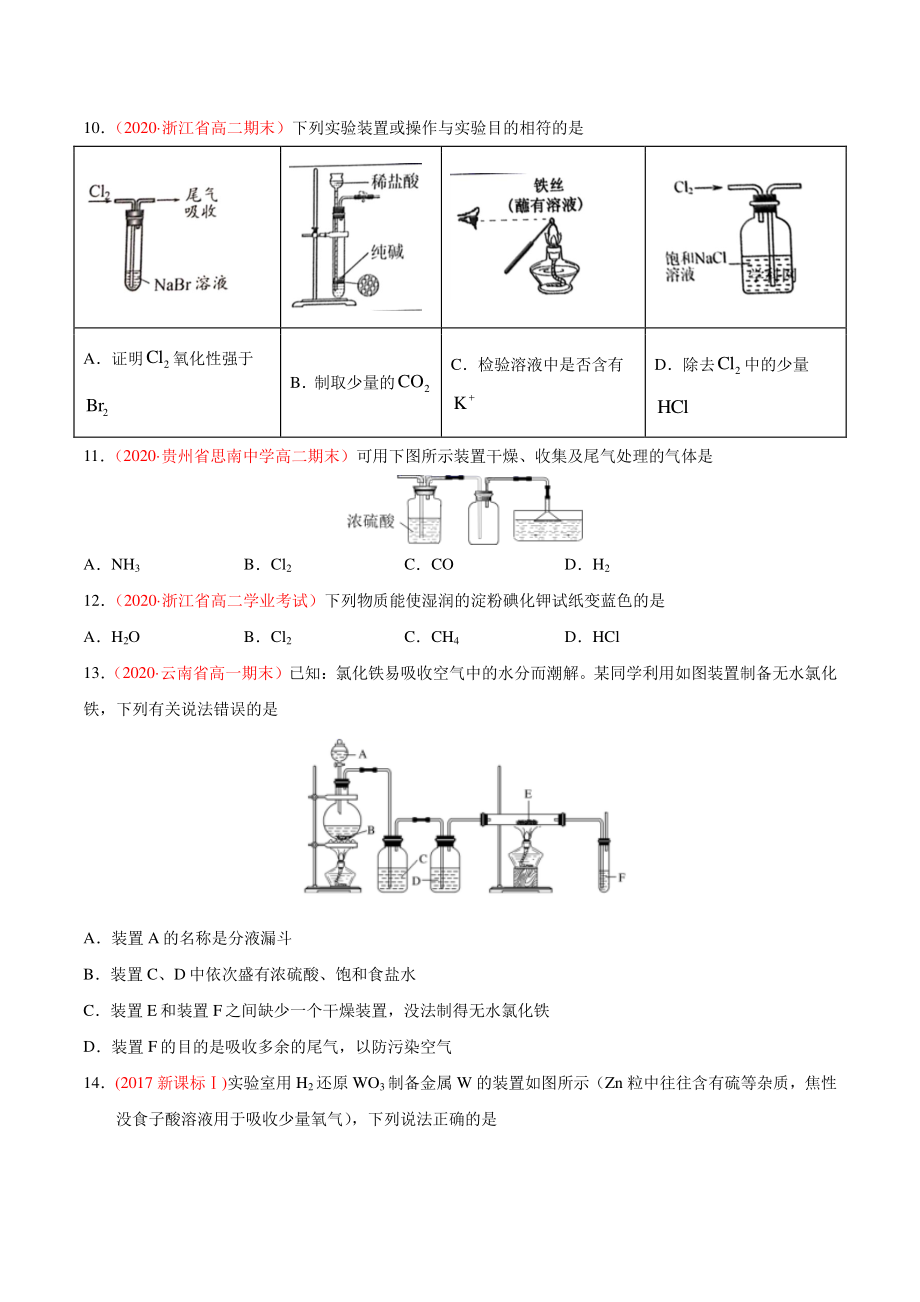
5、碱石灰除去氯气中含有的水分 C用澄清石灰水鉴别 CO和 CO2 D金属钠着火时,可用细沙覆盖灭火 10 (2020 浙江省高二期末)下列实验装置或操作与实验目的相符的是 A证明 2 Cl氧化性强于 2 Br B制取少量的 2 CO C检验溶液中是否含有 K D除去 2 Cl中的少量 HCl 11 (2020 贵州省思南中学高二期末)可用下图所示装置干燥、收集及尾气处理的气体是 ANH3 BCl2 CCO DH2 12 (2020 浙江省高二学业考试)下列物质能使湿润的淀粉碘化钾试纸变蓝色的是 AH2O BCl2 CCH4 DHCl 13 (2020 云南省高一期末)已知:氯化铁易吸收空气中的水
6、分而潮解。某同学利用如图装置制备无水氯化 铁,下列有关说法错误的是 A装置 A的名称是分液漏斗 B装置 C、D中依次盛有浓硫酸、饱和食盐水 C装置 E和装置 F之间缺少一个干燥装置,没法制得无水氯化铁 D装置 F的目的是吸收多余的尾气,以防污染空气 14(2017 新课标)实验室用 H2还原 WO3制备金属 W 的装置如图所示(Zn 粒中往往含有硫等杂质,焦性 没食子酸溶液用于吸收少量氧气) ,下列说法正确的是 A、中依次盛装 KMnO4溶液、浓 H2SO4、焦性没食子酸溶液 B管式炉加热前,用试管在处收集气体并点燃,通过声音判断气体纯度 C结束反应时,先关闭活塞 K,再停止加热 D装置 Q(
7、启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气 二、非选择题二、非选择题 15 (2020 日喀则市拉孜高级中学高一期末)二氧化锰( 2 MnO)与浓盐酸混合加热可得到氯气,如图是制取 2 Cl并探究化学性质的装置图。 (1)圆底烧瓶中发生反应的化学方程式为_。 (2)若要得到干燥纯净的气体,则 B 中应盛放的试剂是_,作用是_;C中应盛放的试剂是 _,作用是_。 (3)E 中若装有淀粉碘化钾溶液,能观察到的实验现象是_。 (4) 2 Cl的密度比空气_,且_(填“能”或“不能”)溶于水,难溶于饱和食盐水,因此可用_法或排 饱和食盐水法收集。 (5)G中的试剂可为_。 16 (2020 河北
8、深州市中学高一期末)该研究性学习小组为了探究在实验室制备 Cl2的过程中有水蒸气和 HCl 挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略) 已 知:Cl2易溶于 CCl4而 HCl 不溶于 CCl4 按要求回答问题: (1)写出装置 A制取 Cl2的化学方程式_。 (2)装置 B中的试剂是_,现象是_。 (3)装置 D和 E中出现的不同现象说明的问题是_。 (4)装置 F的作用是_。 (5)乙同学认为甲同学的实验有缺陷,不能确保最终通入 AgNO3溶液中的气体只有一种,为了确保实验结 论的可靠性, 证明最终通入 AgNO3溶液的气体只有一种, 乙同学提出
9、在 F和 G 之间再连接一个洗气瓶装置, 则装置中应放入_(填写试剂或用品名称) ,改正后证明有 HCl 挥发出来的现象是_。 第二章 海水中的重要元素钠和氯 第二节第二节 氯及其化合物氯及其化合物 第第 3 课时课时 氯气的制备氯气的制备 一、选择题一、选择题 1 (2019 福建省尤溪第一中学高一月考)下列关于氯及其化合物的叙述正确的是( ) A氯气的性质很活泼,它与氢气混合后立即发生爆炸 B实验室制取氯气时,为了防止环境污染,多余的氯气可以用饱和食盐水吸收 C久置的氯水没有漂白性 D检验 HCl 气体中是否混有 2 Cl的方法是将气体通入硝酸银溶液 【答案】C 【解析】A. 氯气的性质很
10、活泼,它与氢气混合后在关照的条件下发生爆炸,故 A 错误;B. 实验室制取氯气 时, 为了防止环境污染, 多余的氯气可以用氢氧化钠溶液吸收, 故 B 错误;C. 久置的氯水中,次氯酸分解, 没有漂白性,故 C 正确;D. HCl 气体及 2 Cl通入硝酸银溶液,均能生成白色氯化银沉淀,故 D 错误;故选 C。 2下列离子方程式的书写正确的是( ) A实验室用大理石和稀盐酸制取 CO2:2H+CO32-=CO2+H2O B钠与水反应:Na+2H2O=Na+2OH-+H2 C将稀硫酸滴在铜片上: Cu+2H+=Cu2+H2 D有效成分为NaClO的消毒液与有效成分为浓HCl的洁厕灵混用产生黄绿色气
11、体: 22 ClOCl2H =ClH O 【答案】D 【解析】A. 大理石是碳酸钙,不溶于水,不能拆成离子形式,故离子方程式 2H+CO32-=CO2+H2O是错 误的,故错误;B. 电荷不守恒,应为:2Na+2H2O=2Na+2OH-+H2,A 项错误;C. 铜与稀硫酸不反应,故 错误;D二者在酸性条件下发生氧化还原反应,离子方程式符合反应事实,遵循电子守恒、电荷守恒、原 子守恒,D正确;故合理选项是 D。 3 (2020 衡东县欧阳遇实验中学高一期末)下列除去杂质的实验方法正确的是 A除去 Cl2中的少量 HCl:通过饱和 NaHCO3溶液,收集气体 B除去 K2CO3固体中少量 NaHC
12、O3:置于坩埚中加热 C除去 KCl溶液中的少量 MgCl2:加入适量 NaOH溶液,过滤 D除去氢氧化铁胶体中的 Cl:渗析 【答案】D 【解析】A. Cl2通过饱和 NaHCO3溶液,发生反应 Cl2+H2OHCl+HClO,NaHCO3+HCl=NaCl+CO2+H2O, 因此氯气会被饱和 NaHCO3溶液吸收,故 A错误;B. NaHCO3受热分解生成 Na2CO3,因此不能得到纯净的 K2CO3,故 B错误;C. 加入适量 NaOH溶液生成 NaCl,引入新杂质,故 C错误;D. 胶体粒子不能透过半 透膜,而离子能透过半透膜,故除去氢氧化铁胶体中的 Cl-可用渗析的方法,故 D 正确
13、,故选 D。 4 (2020 云南省高一期末)实验室用浓盐酸和二氧化锰制氯气。下列说法错误的是 A浓盐酸在该反应中表现出酸性和还原性 B该方法是瑞典化学家舍勒最先发现的 C该反应的氧化产物是二氯化锰,还原产物是氯气 D该反应的离子方程式为 MnO2+4H+2Cl- Mn2+Cl2+2H2O 【答案】C 【解析】实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为: MnO2+4HCl(浓) MnCl2+Cl2+2H2O,据此回答问题。A.有分析中的方程式可知,一部分氯元素的化合 价从-1 价升高到 0价,作还原剂,具有还原性,还有一部分氯元素的化合价没有变化,生成盐和水,所以
14、浓盐酸在该反应中表现出酸性和还原性, 故 A正确, 但不符合题意; B. 实验室用浓盐酸和二氧化锰制氯气, 是瑞典化学家舍勒最先发现的,故 B正确,但不符合题意;C. 该反应的氧化产物是氯气,还原产物是二氯 化锰,故 C错误,符合题意;D.二氧化锰和水是氧化物,不能拆成离子的形式,氯化氢和氯化锰是可溶于 水的强电解质,拆成离子的形式,氯气是单质,写化学式,该反应的离子方程式为 MnO2+4H+2Cl- Mn2+Cl2+2H2O,符合电荷守恒,客观事实,原子守恒,故 D正确,但不符合题意; 故选:C。 5 (2020 营口市第二高级中学高一期末)实验室里可按下图所示的装置来干燥、收集气体 R,多


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第二节 氯及其化合物第3课时氯气的制备 作业练习含答案 第二 及其 化合物 课时 氯气 制备 作业 练习 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-192408.html