 2020-2021年高考化学真题分项版汇编 专题13 元素及其化合物知识的综合应用(学生版)
2020-2021年高考化学真题分项版汇编 专题13 元素及其化合物知识的综合应用(学生版)
《2020-2021年高考化学真题分项版汇编 专题13 元素及其化合物知识的综合应用(学生版)》由会员分享,可在线阅读,更多相关《2020-2021年高考化学真题分项版汇编 专题13 元素及其化合物知识的综合应用(学生版)(5页珍藏版)》请在七七文库上搜索。
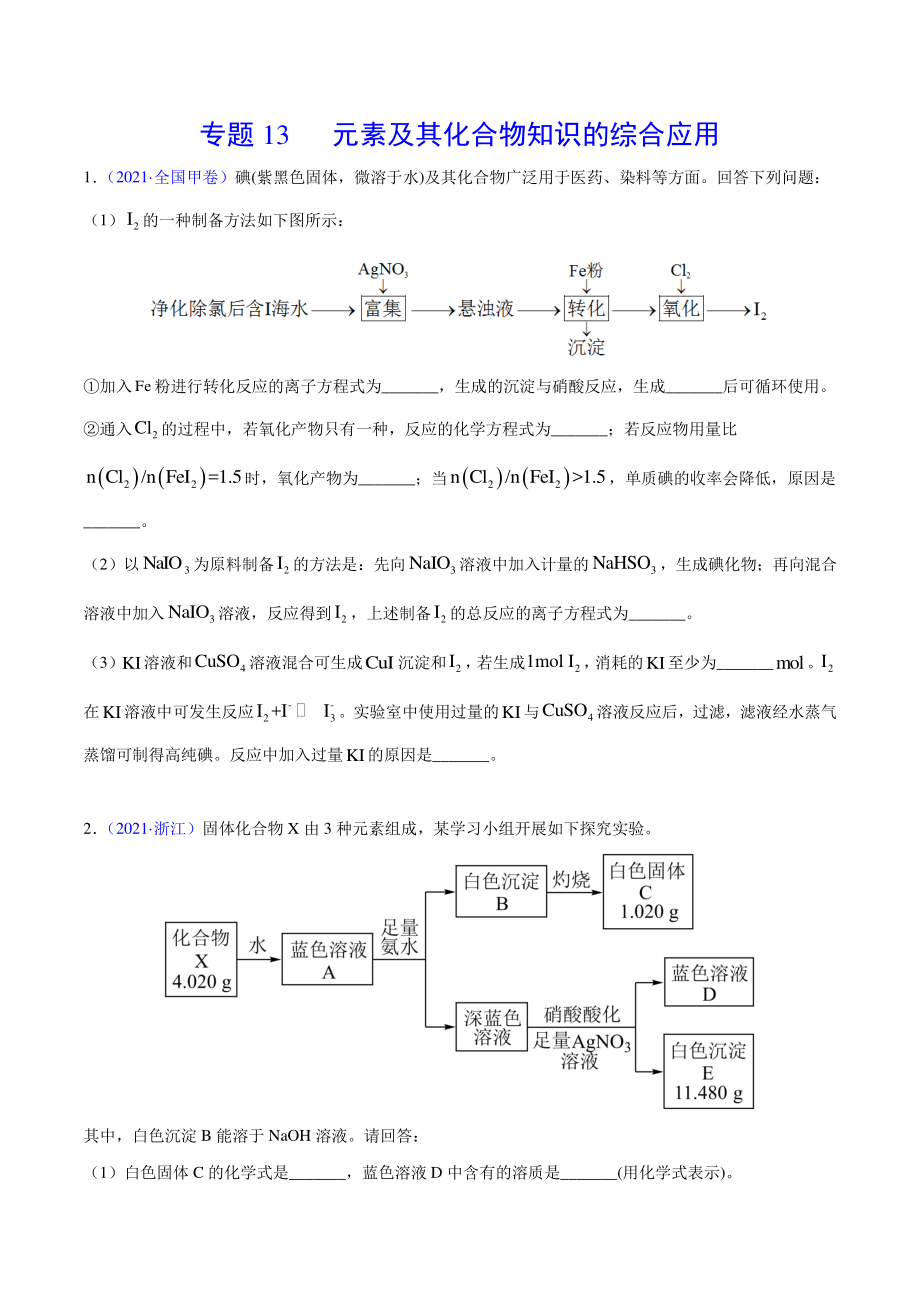
1、专题 13 元素及其化合物知识的综合应用 1 (2021 全国甲卷)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列问题: (1) 2 I的一种制备方法如下图所示: 加入Fe粉进行转化反应的离子方程式为_,生成的沉淀与硝酸反应,生成_后可循环使用。 通入 2 Cl的过程中,若氧化产物只有一种,反应的化学方程式为_;若反应物用量比 22 n Cl/n FeI=1.5时,氧化产物为_;当 22 n Cl/n FeI1.5,单质碘的收率会降低,原因是 _。 (2)以 3 NaIO为原料制备 2 I的方法是:先向 3 NaIO溶液中加入计量的 3 NaHSO,生成碘化物;再向混合
2、 溶液中加入 3 NaIO溶液,反应得到 2 I,上述制备 2 I的总反应的离子方程式为_。 (3)KI溶液和 4 CuSO溶液混合可生成CuI沉淀和 2 I, 若生成 2 1mol I, 消耗的KI至少为_mol。 2 I 在KI溶液中可发生反应 - 23 I +II。实验室中使用过量的KI与 4 CuSO溶液反应后,过滤,滤液经水蒸气 蒸馏可制得高纯碘。反应中加入过量KI的原因是_。 2 (2021 浙江)固体化合物 X 由 3 种元素组成,某学习小组开展如下探究实验。 其中,白色沉淀 B 能溶于 NaOH 溶液。请回答: (1)白色固体 C 的化学式是_,蓝色溶液 D 中含有的溶质是_(
3、用化学式表示)。 (2)化合物 X 的化学式是_;化合物 X 的一价阴离子与 CH4具有相同的空间结构,写出该阴离子的 电子式_。 (3)蓝色溶液 A 与 + 25 N H作用,生成一种气体,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀。 写出该反应的离子方程式_。 设计实验验证该白色沉淀的组成元素_。 3 (2021 浙江)某兴趣小组对化合物 X 开展探究实验。 其中:X 是易溶于水的强酸盐,由 3 种元素组成;A 和 B 均为纯净物;B 可使品红水溶液褪色。请回答: (1)组成 X 的 3 种元素是_(填元素符号),X 的化学式是_。 (2)将固体 X 加入温热的稀 H2SO4中,产生气体
4、B,该反应的离子方程式是_。 (3)步骤 I,发生反应的化学方程式是_。 (4)步骤 II,某同学未加 H2O2溶液,发现也会缓慢出现白色浑浊,原因是_。 (5)关于气体 B 使品红水溶液褪色的原因,一般认为:B 不能使品红褪色,而是 B 与水反应的生成物使品 红褪色。请设计实验证明_。 1(2020 年新课标)化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料, 又是高效、广谱的灭菌消毒剂。回答下列问题: (1)氯气是制备系列含氯化合物的主要原料, 可采用如图(a)所示的装置来制取。 装置中的离子膜只允许_ 离子通过,氯气的逸出口是_(填标号)。 2020 年高考真题年
5、高考真题 (2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数 (X)= - cX cHClO +cClO ( ) () () ,X 为 HClO 或 ClO与 pH 的关系如图(b)所示。HClO 的电离常数 Ka值为_。 (3)Cl2O 为淡棕黄色气体,是次氯酸的酸酐,可由新制的 HgO 和 Cl2反应来制备,该反应为歧化反应(氧化剂 和还原剂为同一种物质的反应)。上述制备 Cl2O 的化学方程式为_。 (4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为 NaClO2、NaHSO4、 NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2020-2021年高考化学真题分项版汇编 专题13 元素及其化合物知识的综合应用学生版 2020 2021 年高 化学 真题分项版 汇编 专题 13 元素 及其 化合物 知识 综合 应用 学生
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-188821.html