 湖北省随州市2021年中考化学试题(解析版)
湖北省随州市2021年中考化学试题(解析版)
《湖北省随州市2021年中考化学试题(解析版)》由会员分享,可在线阅读,更多相关《湖北省随州市2021年中考化学试题(解析版)(13页珍藏版)》请在七七文库上搜索。
1、 随州市随州市 2021 年初中毕业升学考试理科綜合试题年初中毕业升学考试理科綜合试题 可能用到的相对原子质量:可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Zn-65 第第卷(选择题共卷(选择题共 60 分)分) 第第卷共卷共 25 题,每题只有一个选项最符合题意。题,每题只有一个选项最符合题意。17 题为生物题,题为生物题,815 题为化学题,题为化学题,16-25 题为物理题。题为物理题。115 题每题题每题 2 分,分,16-25 题每题题每题 3 分。分。 1. 生活中处处有化学,下列变化不涉及化学变化的是 A. 用水银体温计测量体温 B. 服用碱性药物治疗
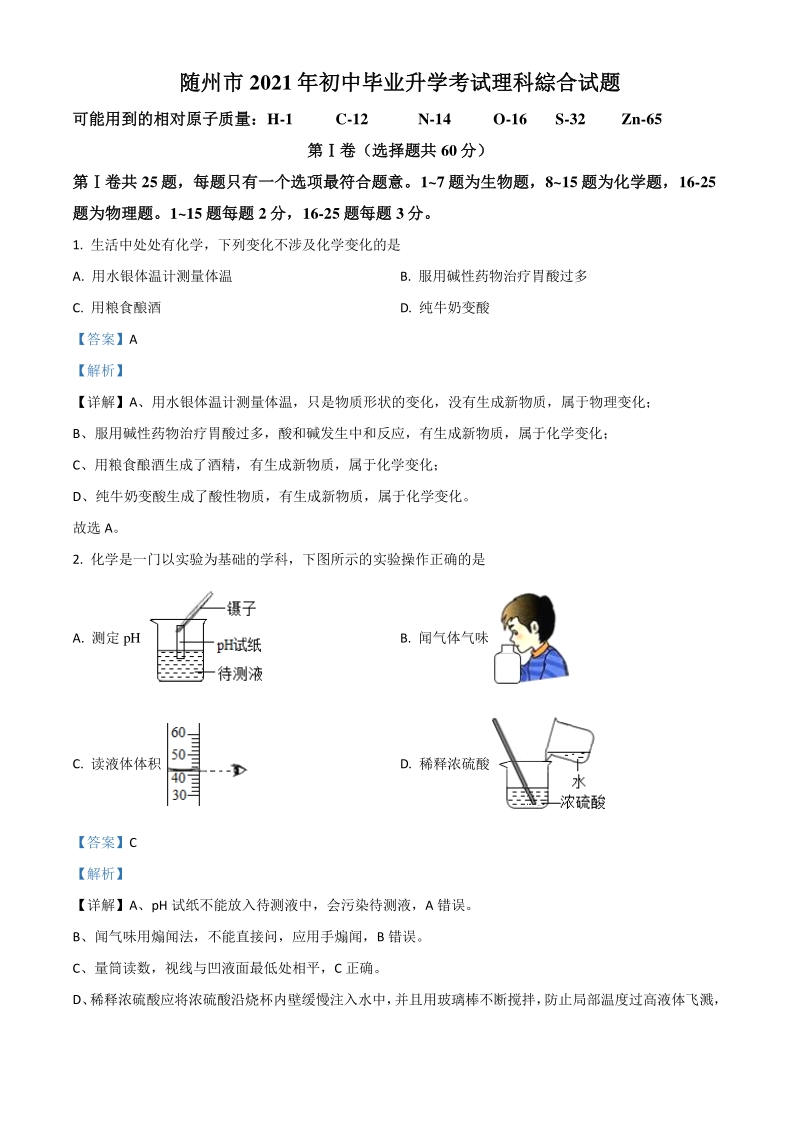
2、胃酸过多 C. 用粮食酿酒 D. 纯牛奶变酸 【答案】A 【解析】 【详解】A、用水银体温计测量体温,只是物质形状的变化,没有生成新物质,属于物理变化; B、服用碱性药物治疗胃酸过多,酸和碱发生中和反应,有生成新物质,属于化学变化; C、用粮食酿酒生成了酒精,有生成新物质,属于化学变化; D、纯牛奶变酸生成了酸性物质,有生成新物质,属于化学变化。 故选 A。 2. 化学是一门以实验为基础的学科,下图所示的实验操作正确的是 A. 测定 pH B. 闻气体气味 C. 读液体体积 D. 稀释浓硫酸 【答案】C 【解析】 【详解】A、pH 试纸不能放入待测液中,会污染待测液,A 错误。 B、闻气味用煽
3、闻法,不能直接问,应用手煽闻,B 错误。 C、量筒读数,视线与凹液面最低处相平,C 正确。 D、 稀释浓硫酸应将浓硫酸沿烧杯内壁缓慢注入水中, 并且用玻璃棒不断搅拌, 防止局部温度过高液体飞溅, D 错误。 故选:C。 3. “宏观一微观一符号”是学习化学的重要内容和方法。甲图表示镓在元素周期表中的部分信息和核外电 子排布情况,乙图 A、B、C表示部分原子核外电子排布情况,据图所得信息描述正确的是 A. 镓的相对原子质量为 69.72g B. 镓是一种金属元素 C. 图 C表示的是一种阳离子 D. 氯化镓的化学式为 GaCl2 【答案】B 【解析】 【详解】A、根据元素周期表一格的信息可知,元
4、素名称下方的数字表示相对原子质量,镓的相对原子质量 为 69.72,相对原子质量单位是“1”,不是“g”,A 错误; B、镓带“钅”字旁,属于金属元素,B 正确; C、图 C 中核电荷数为 17,小于核外电子数 2+8+8=18,属于阴离子,C 错误; D、 镓最外层电子数是 3, 容易失去 3 个电子, 形成带 3 个单位正电荷的阳离子, 在化合物中化合价为+3 价, 氯元素化合价为-1 价,氯化镓的化学式为 GaCl3,D 错误。 故选 B。 4. 归纳法是一种重要的学习方法,可将零碎的知识结构化,系统化,下列归纳都正确的是 A 化学与生活 B化学与材料 1、制糖工业中利用活性炭脱色制白糖
5、 2、衣服上的油污用洗涤剂和汽油都能除去, 其去污原理是一样的 3、氮肥、磷肥、钾肥是重要的化学肥料 1、涤轮衣服优点是吸湿透气性好 2、Fe2O3、CuO属于合金 3、鸡蛋提供的营养主要是蛋白质 C化学与安全 D化学与环保 1、点燃可燃性气体前,一定要验纯 2、煤矿井中一定要通风,严禁烟火 3、炒菜时油锅起火,立即盖上钢盖 1、为防止温室效应推广使用脱硫煤 2、生活垃圾应分类处理 3、废旧电池可以随手丢弃 A. A B. B C. C D. D 【答案】C 【解析】 【分析】本题考查生活中的基本常识。 【详解】A、加入洗涤剂是利用乳化作用除去油污,加入汽油是利用相似相溶原理进行除去,原理不一
6、样, 故 A 不符合题意; B、涤纶属于合成纤维材料,透气性差,三氧化二铁、氧化铜都属于氧化物,不是合金,故 B 不符合题意; C、点燃可燃气体前需要验纯,否则会发生爆炸,煤矿中含有瓦斯气,遇到明火会爆炸,因此要禁止明火, 炒菜时着火盖上锅盖,是利用隔绝氧气灭火,故 C符合题意; D、废旧电池不能随手丢弃,会污染环境,故 D 不符合题意; 故选 C。 【点睛】本题难度不大,注意生活常识的积累。 5. 化学学习常用化学思维去认识和理解世界,下列说法错误的个数有 物质 甲 乙 丙 丁 反应前质量/g 10 5 12 20 反应后质量/g 8 5 30 x (1)反应中甲和丙的质量比为 1:8 (2
7、)x=4 (3)该反应为化合反应 (4)乙可能是催化剂 (5)若甲与丁的化学计量数之比为 2:3;则其相对分子质量之比为 3:16。 A. 1个 B. 2个 C. 3个 D. 4个 【答案】D 【解析】 【分析】根据质量守恒定律,10+5+12+20=8+5+30+x,x=4; 【详解】 (1)反应中甲和丙质量比为(10-8):(30-12)=1:9,错误; (2)x=4,正确; (3)该反应中甲、丁质量减少为反应物,丙质量增加为生成物,反应符合多变一特点,为化合反应,正确; (4)乙质量反应前后不变,可能不参与反应、可能是催化剂,正确; (5)反应的甲与丁质量比为(10-8):(20-4)=
8、1:8;若甲与丁的化学计量数之比为 2:3;设甲、丁相对分子 质量分别为 a、b,则有 2a 3b = 1 8 ,解得 a b = 3 16 ,正确; 故选 D。 6. 除杂和提纯是化学的基本实验技能之一,下列实验操作能达到实验目的的是 选项 物质 所含杂质 加入的试剂和操 作 A CO2 CO 点燃 B N2 O2 灼热的铜网 C CuCl2溶液 FeCl2 加入适量铁粉, 过 滤 D CaO CaCO3 适量的稀盐酸 A. A B. B C. C D. D 【答案】B 【解析】 【详解】A、二氧化碳不燃烧也不助燃,常用来灭火,故当二氧化碳中含有杂质一氧化碳时,点不燃,应通 过灼热的氧化铜网
9、来除去一氧化碳,A 操作错误; B、灼热的铜网可与氧气反应生成固体氧化铜,但不与氮气反应,B 操作正确; C、铁比铜活泼,故铁可将氯化铜中的铜置换出来,生成氯化亚铁,反而把原物质除去,不符合除杂原则, C 操作错误; D、盐酸可与氧化钙反应生成氯化钙和水,与碳酸钙反应生成氯化钙、水和二氧化碳,反而把原物质除去, 不符合除杂原则,D 操作错误。 故选 B。 7. “证据推理与模型认知”是化学学科核心素养的重要组成部分,以下推理正确的是 A. 中和反应生成盐和水,所以生成盐和水的反应都是中和反应 B. 单质只含有一种元素,所以只含有一种元素的物质一定是单质 C. 燃烧都伴随有发光放热现象,所以有发
10、光放热现象的一定是燃烧 D. NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液 【答案】D 【解析】 【详解】A、中和反应生成盐和水,生成盐和水的反应不都是中和反应,例如氢氧化钙和二氧化碳生成盐和 水,错误; B、单质只含有一种元素,只含有一种元素的物质不一定是单质,例如氧气和臭氧组成的混合物,错误; C、燃烧都伴随有发光放热现象,有发光放热现象的不一定是燃烧,例如白炽灯发光发热,错误; D、NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液,正确。 故选 D。 8. 图像能直观体现化学中的各种变化关系,加深对化学知识的
11、理解。下列图像能正确表示对应叙述的有 A. 向氢氧化钠溶液中加水稀释 B. 向一定量的盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液 C. 电解水生成氢气和氧气的质量与反应时间的关系 D. 向等质量的 Zn、Fe 中滴加等浓度等质量的稀盐酸 【答案】D 【解析】 【详解】A、氢氧化钠溶液显碱性,加水稀释时,碱性越来越弱,最后趋近于中性,故 pH 从大变小,最后 趋近于 7,但不可能小于 7,A 错误; B、盐酸和硫酸钠的混合液中加入氢氧化钡时,氢氧根离子会和氢离子反应生成水,钡离子和硫酸根离子反 应生成硫酸钡沉淀,两个反应互不干扰,故沉淀是从 0 点开始增加的,B 错误; C、电解水生成的氢气和
12、氧气的质量比为 1:8,体积比为 2:1,C 错误; D、向等质量的两种活泼金属中滴加酸时,刚开始滴加酸的速率相同且酸不足,氢气的质量由酸决定,故两 种金属产生氢气的速率和质量相同;当酸过量时,氢气质量由金属决定;二价的铁和锌与酸反应产生的氢 气和其相对原子质量成反比,铁和锌的相对原子质量分别是 56 和 65,故铁产生的氢气更多一些,D 正确; 故选 D。 第第卷(非选择题共卷(非选择题共 90 分)分) 2635 题为物理题,题为物理题,3642 题为化学题,题为化学题,4345 题为生物题。题为生物题。 9. 请从 H、O、C、N、Cu、Na 六种元素中选择合适的元素,用化学用语填空:
13、(1)两个氢原子_; (2)铵根离子_; (3)碳酸钠中碳元素的化合价_; (4)含氧量最高氧化物_; (5)属于有机氮肥的是_; (6)有蓝色沉淀生成的复分解反应_。 【答案】 (1). 2H (2). NH4+ (3). +4 23 Na CO (4). H2O2 (5). CO(NH2)2 (6). 3 223 Cu(NO ) +2NaOH=Cu(OH)+2NaNO 【解析】 【分析】 【详解】 (1)原子的表示方法是用元素符号来表示一个原子,表示多个该原子,在其元素符号前加上相应 的数字。两个氢原子表示为:2H; (2)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负
14、电荷数,数字在前,正负 符号在后,带 1 个电荷时,1 要省略。表示多个该离子,就在其元素符号前加上相应的数字。铵根离子表示 为:NH4+; (3)碳酸钠中,氧是-2 价,钠是+1 价,根据化合价代数和为 0,求得碳是+4价。元素化合价的表示方法: 确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在 前,数字在后。化合价在表示时写在元素符号的正上方,所以表示为: +4 23 Na CO ; (4)氧化物中,氧元素含量最高的物质是过氧化氢,化学式为:H2O2; (5)氮肥是含有氮元素的化肥,有机氮肥为尿素:CO(NH2)2; (6)蓝色沉淀是氢氧化铜,所
15、以反应可以是硝酸铜和氢氧化钠的反应: 3 223 Cu(NO ) +2NaOH=Cu(OH)+2NaNO。 【点睛】 10. 学习化学更重要是学会用化学观点去分析、解决生产生活中的问题。 (1)水是生命之源。但是硬水不仅对健康造成危害,而且会给生活带来很多麻烦和诸多危害,生活上可以 用_来区分硬水和软水。 (2)精准扶贫使农村生活发生了翻天覆地的变化,广大农村地区也使用上了清洁的天然气作为燃料。天然 气使用后关闭阀门即可灭火,其原理是_。 (3) 2021 年 1月 1日起, 全国餐饮行业全面禁止使用一次性不可降解塑料吸管, “禁管令”就此诞生。 “禁 管令”可有效缓解的环境问题是_。 A白色


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 湖北省 随州市 2021 年中 化学试题 解析
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
文档标签
- 化学试题
- 湖北省随州市2021年中考历史试卷答案及解析
- 江西省2021年中考化学试题解析版
- 湖南省湘潭市2021年中考化学试题解析版
- 湖北省随州市2021年中考语文试题解析版
- 浙江省宁波市2021年中考化学试题解析版
- 浙江省绍兴市2021年中考化学试题解析版
- 湖北省宜昌市2021年中考英语试题解析版
- 湖南省常德市2021年中考化学试题解析版
- 2020年湖北省黄冈市中考化学试题解析版
- 湖北省恩施2021年中考化学试题解析版
- 湖北省随州市2019年中考语文试卷解析版
- 湖南省怀化市2021年中考化学试题解析版
- 湖北省黄石市2021年中考化学试题解析版
- 2020年湖北省鄂州市中考化学试题解析版
- 湖北省随州市2021年中考英语试题解析版
- 湖北省随州市2021年中考语文试题含答案
- 湖北省荆州市2021年中考语文试题解析版
- 2020年湖北省宜昌市中考化学试题解析版
- 湖北省荆州市2021年中考化学试题解析版



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-186492.html