 2020年秋沪教版九年级上册化学第4章检测题(含答案)
2020年秋沪教版九年级上册化学第4章检测题(含答案)
《2020年秋沪教版九年级上册化学第4章检测题(含答案)》由会员分享,可在线阅读,更多相关《2020年秋沪教版九年级上册化学第4章检测题(含答案)(7页珍藏版)》请在七七文库上搜索。
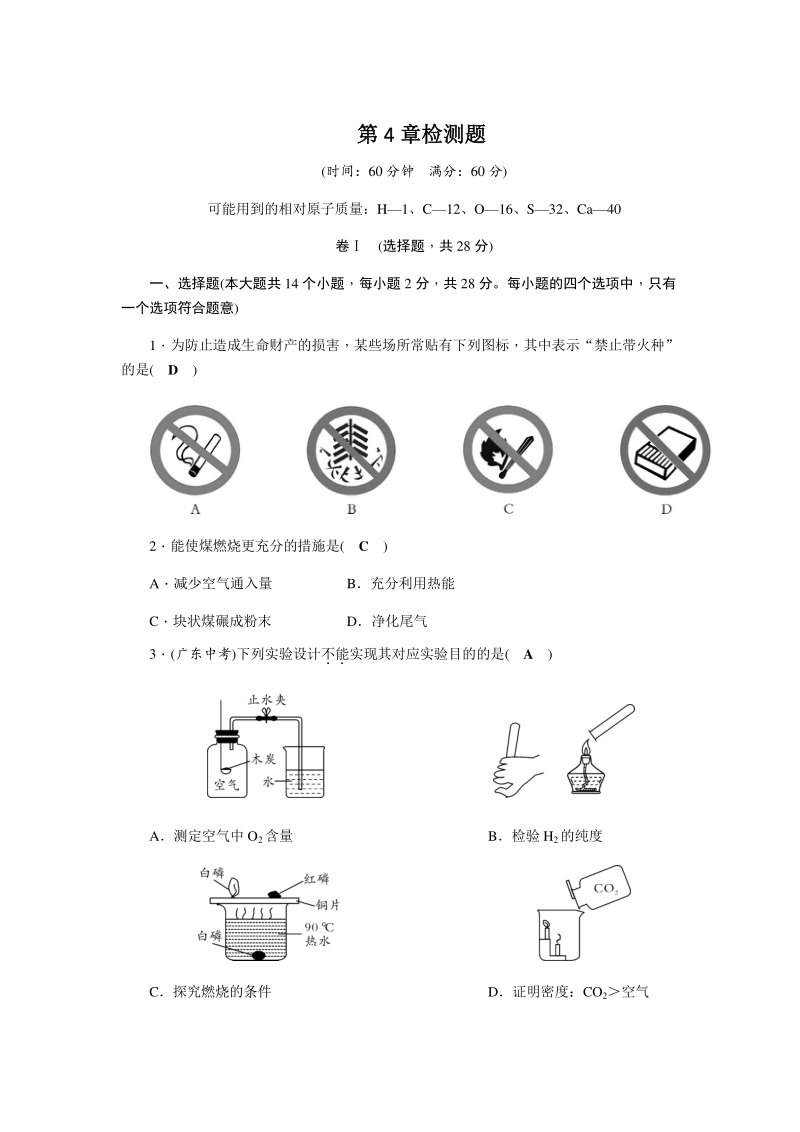
1、 第第 4 4 章检测题章检测题 (时间:60 分钟 满分:60 分) 可能用到的相对原子质量:H1、C12、O16、S32、Ca40 卷 (选择题,共 28 分) 一、选择题(本大题共 14 个小题,每小题 2 分,共 28 分。每小题的四个选项中,只有 一个选项符合题意) 1为防止造成生命财产的损害,某些场所常贴有下列图标,其中表示“禁止带火种” 的是( D ) 2能使煤燃烧更充分的措施是( C ) A减少空气通入量 B充分利用热能 C块状煤碾成粉末 D净化尾气 3(广东中考)下列实验设计不能 实现其对应实验目的的是( A ) A测定空气中 O2含量 B检验 H2的纯度 C探究燃烧的条件
2、D证明密度:CO2空气 4下列说法不正确 的是( B ) A燃烧都放出热量 B红磷常温下在空气中能自燃 C炒菜油锅着火用锅盖盖灭 D木材燃烧必须达到木材的着火点 5如图是某同学探究燃烧条件的设计方案,下列有关说法中不正确的是( C ) A甲图可探究可燃物的燃烧是否需要与氧气接触 B甲图可探究可燃物的燃烧是否需要达到一定温度 C乙图 A 与 C 试管(C 中白磷未燃)比较可探究可燃物的燃烧是否需要达到一定温度 D乙图比甲图更利于环境保护 6化学反应前后,下列各项中,肯定没有变化的是( A ) 原子数目 原子的种类 分子数目 分子的种类 元素的种类 物质的总质量 物质的种类 A B C D 7(上
3、海中考)根据化学方程式:2H2O= 通电 2H2O2,无法获取的信息是( D ) A反应所需条件 B生成物的状态 C生成物的物质的量之比 D氧气可助燃 8下列化学方程式书写正确的是( C ) AFe3O2= 点燃 2Fe2O3 B2P5O2= 点燃 2P2O5 C4Al3O2= 点燃 2Al2O3 D2C2H25O2= 点燃 4CO22H2O 9碳在氧气中燃烧,符合质量守恒定律的是( D ) A8 g 碳和 14 g 氧气反应生成 22 g 二氧化碳 B11 g 碳和 11 g 氧气反应生成 22 g 二氧化碳 C12 g 碳和 10 g 氧气反应生成 22 g 二氧化碳 D3 g 碳和 8
4、g 氧气反应生成 11 g 二氧化碳 10(安徽中考)下列实验事实不能 作为相应观点的证据的是( D ) 选项 实验事实 观点 A 铁丝在氧气中燃烧后质量增大 化学反应前后质量守恒 B 水电解可得到氢气和氧气 分子是可分的 C 少量白糖加入水中,不久“消失” 微粒是不断运动的 D 5 mL 苯和 5 mL 冰醋酸混合后体积大于 10 mL 微粒间有间隔 11.科学家发现,利用催化剂可有效消除室内装修材料释放的甲醛,其反应的微观示意 图如下。下列有关该反应的说法正确的是( B ) A属于置换反应 B可解决甲醛带来的室内空气污染问题 C其中甲醛属于氧化物 D化学方程式为:HCOO2=CO2H2O
5、12实验室用 16 g 高锰酸钾放在试管中加热,反应后称得剩余物质的质量为 14.4 g,则 剩余的物质是( B ) AK2MnO4 BMnO2、K2MnO4、KMnO4 CMnO2和 K2MnO4 DKMnO4和 K2MnO4 13(河北中考)一定条件下,密闭容器内发生某化学反应,测得 t1 s 和 t2 s 时各物质的 质量见下表。下列说法正确的是( D ) 物质 M N P Q t1 s 时的质量/g 51 9 3 17 t2 s 时的质量/g 23 3 x 51 A.x 的值小于 3 BQ 可能是单质 C该反应一定是分解反应 DM 与 N 的质量变化之比为 143 14现有 32 g


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2020 年秋沪教版 九年级 上册 化学 检测 答案
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-152141.html