 福建省莆田市2020年中考化学二模试卷(含答案解析)
福建省莆田市2020年中考化学二模试卷(含答案解析)
《福建省莆田市2020年中考化学二模试卷(含答案解析)》由会员分享,可在线阅读,更多相关《福建省莆田市2020年中考化学二模试卷(含答案解析)(13页珍藏版)》请在七七文库上搜索。
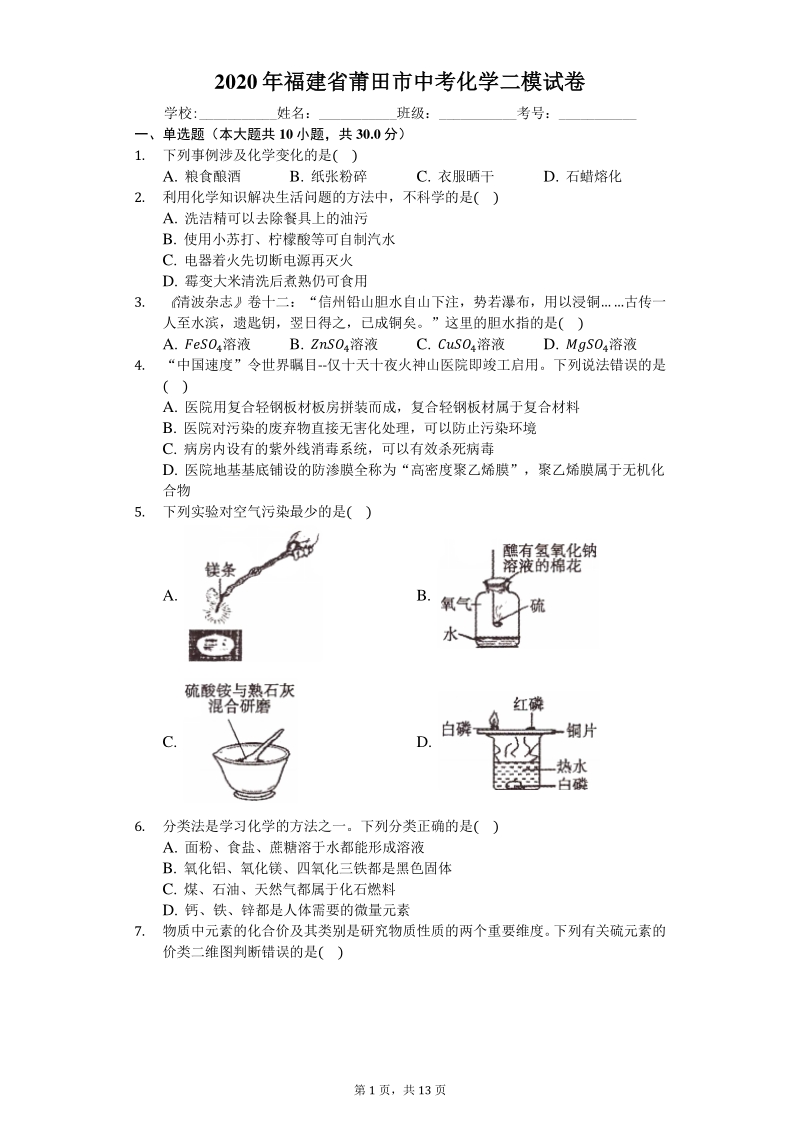
1、第 1 页,共 13 页 2020 年福建省莆田市中考化学二模试卷年福建省莆田市中考化学二模试卷 学校:_姓名:_班级:_考号:_ 一、单选题(本大题共 10 小题,共 30.0 分) 1. 下列事例涉及化学变化的是( ) A. 粮食酿酒 B. 纸张粉碎 C. 衣服晒干 D. 石蜡熔化 2. 利用化学知识解决生活问题的方法中,不科学的是( ) A. 洗洁精可以去除餐具上的油污 B. 使用小苏打、柠檬酸等可自制汽水 C. 电器着火先切断电源再灭火 D. 霉变大米清洗后煮熟仍可食用 3. 清波杂志卷十二:“信州铅山胆水自山下注,势若瀑布,用以浸铜古传一 人至水滨,遗匙钥,翌日得之,已成铜矣。”这里
2、的胆水指的是( ) A. 4溶液 B. 4溶液 C. 4溶液 D. 4溶液 4. “中国速度”令世界瞩目-仅十天十夜火神山医院即竣工启用。下列说法错误的是 ( ) A. 医院用复合轻钢板材板房拼装而成,复合轻钢板材属于复合材料 B. 医院对污染的废弃物直接无害化处理,可以防止污染环境 C. 病房内设有的紫外线消毒系统,可以有效杀死病毒 D. 医院地基基底铺设的防渗膜全称为“高密度聚乙烯膜”,聚乙烯膜属于无机化 合物 5. 下列实验对空气污染最少的是( ) A. B. C. D. 6. 分类法是学习化学的方法之一。下列分类正确的是( ) A. 面粉、食盐、蔗糖溶于水都能形成溶液 B. 氧化铝、氧
3、化镁、四氧化三铁都是黑色固体 C. 煤、石油、天然气都属于化石燃料 D. 钙、铁、锌都是人体需要的微量元素 7. 物质中元素的化合价及其类别是研究物质性质的两个重要维度。 下列有关硫元素的 价类二维图判断错误的是( ) 第 2 页,共 13 页 A. W 点所示物质可以通过化合反应生成 X 点所示物质 B. X 点所示物质中硫元素和氧元素的质量比为 1:2 C. Y 点所示物质可用于金属除锈 D. Z点所示物质可以为24 8. 下列说法正确的是( ) A. 一氧化碳具有还原性,可用于冶金工业 B. 氮气在空气中的质量分数约占78% C. 用试管夹夹持试管时,应由试管口往下套 D. 农药有毒,农
4、业生产上应禁止施用 9. 下列图象能正确反映对应关系的是( ) A. 室温下,向氢氧化钙溶液中加水 B. 室温下, 向氢氧化钙饱和溶液中加入氢氧化钙固 体 C. 氢氧化钙在水中的溶解度曲线 D. 室温下,向一定质量的氢氧化钙溶液中加入氧化钙 第 3 页,共 13 页 10. 2的回收利用是环保领域研究的热点。在太阳能的作用下,以2为原料制取炭 黑的流程如图所示。下列判断错误的是( ) A. 2和 FeO 在427发生反应生成 C 和34 B. 34在太阳能等的作用下分解生成 FeO 和2 C. FeO 在反应过程中可以循环使用 D. 该总反应的化学方程式为2= + 2 二、填空题(本大题共 4
5、 小题,共 33.0 分) 11. 化学与生活、社会、环境密切相关。 (1)枇杷味道甜美,营养丰富,有果糖、葡萄糖和维生素等。果糖和葡萄糖属于六 大营养素中的_。 (2)“共享单车绿色出行”。单车的部分构件选用了铝合金材料,其优点是_( 写一条即可);防止其链条生锈的措施是_。 (3)有一种新型催化剂,可以将装修残留在空气中的甲醛(2)与氧气反应转化为 水和二氧化碳,反应的化学方程式为_。 12. 2020年“中国水周”活动的主题为“坚持节水优先,建设幸福河湖”。 (1)图 1中活性炭的作用是_,该装置净化后的水_(填“一定”或“不一 定”)是软水。 (2)检验图 2中气体 a 的方法是_,电
6、解水的化学方程式为_。 (3)图 3说明,该反应中保持不变的粒子是_,分解后生成的氢分子和氧分子 的个数比为_。 (4)节约用水人人有责,举出一种生活中的节水措施_。 13. 垃圾分类回收利用是一种时代新时尚。 (1)过期药品应投放的垃圾箱是_(填序号)。 (2)废旧电池可以回收利用。某品牌干电池的剖面图如图所示。 第 4 页,共 13 页 氯化铵在农业上可用作_肥。 为了验证 Zn和 Cu的金属活动性强弱,除了回收的 Zn 和 Cu 外,请从24、 4和24三种溶液中选择一种完成实验,写出反应的化学方程式_,结 论是_。 废旧电池中金属回收的优点_。 14. 氯化钠是一种重要的化工原料,利用
7、海水可制得氯化钠并进而可以制造氢氧化钠、 氢气和氯气(2)。其主要工艺流程如图所示。 (1)氯原子的结构示意图为, 其核电荷数为_, 在化学反应中该原子 易_(填“得到”或“失去”)电子。 (2)海水在贮水池里待澄清的净水方法是_。 (3)粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。 实验室进行粗盐中难溶性杂质的去除,多步操作需要用到的同一种玻璃仪器是 _。 实验室要除去粗盐中的氯化钙,可加入适量的_(填序号)。 A.23溶液 B.3溶液 C.23溶液 (4)常温下,配制 1000kg质量分数为26.5%的氯化钠饱和溶液,需要氯化钠的质量 为_kg。 (5)电解氯化钠饱
8、和溶液的化学方程式是_。 三、计算题(本大题共 1 小题,共 6.0 分) 15. 有一锅炉内含较多水垢,其主要成分为碳酸钙,为测定其中碳酸钙含量,取5.0样 品加热,加热过程中剩余固体的质量随加热时间的变化如图所示。 已知:3 高温 + 2,假设其他物质不反应。 (1)纵坐标 m点的值为_。 (2)求样品中碳酸钙的质量分数? 第 5 页,共 13 页 四、推断题(本大题共 1 小题,共 8.0 分) 16. A、 B、 C、 D四种物质(或其溶液)分别是 HCl、 NaOH、 4、 CuO中的一种, 它们之间的关系如图所示(反应条件与其他 物质均已略去)。“”表示可以向箭头所指方向一步转化,
9、 “”表示两端的物质可以发生反应。 (1)举出氢氧化钠的一种用途_。 (2)是_。 (3)与 D 反应的化学方程式为_。 (4)可以用_(填一种物质)替代。 五、探究题(本大题共 2 小题,共 23.0 分) 17. 某兴趣小组在实验室利用如图部分装置,制取二氧化碳并验证其性质。 (1)仪器 a 的名称是_。 (2)实验室制取2反应的化学方程式为_,应选择的发生装置是_(填序 号,下同),收集装置是_。 (3)图 F中干燥紫色石蕊纸条的作用是_。 (4)图F实验可以验证2的化学性质有_(写一点即可), 判断依据是_(写 现象)。为了更快观察到现象,其操作方法是_。 (5)若选用 A 装置为高锰
10、酸钾制取氧气的发生装置,其不足之处是_。 18. 某兴趣小组为探究浓硫酸、硅胶和氯化钙的干燥效果,设计了以下两个探究活动。 资料:相对湿度,一定温度下在一定体积的气体中水蒸气的含量。 【活动一】探究浓硫酸的干燥效果。 实验室按图 1所示制取并干燥氧气, 测得用浓硫酸干燥氧气的时间与相对湿度变化 关系如图 2 所示。 第 6 页,共 13 页 (1)用图 1 装置 A完成10%过氧化氢溶液制取氧气的实验,其反应的化学方程式为 _;图 2的曲线表征,开始时产生氧气的速率过快,为了避免反应太剧烈,可 以_。 (2)图 1设计两次浓硫酸干燥氧气的目的是_。 (3)分析图 2的曲线,你能得到的实验结论是
11、_。 【活动二】探究硅胶和氯化钙的干燥效果。 .将装有等体积、等温度的两杯 20mL的水分别放入如图 3 所示的甲、乙两个密闭 容器中,乙的容器中加有 20g硅胶,测出时间与相对湿度变化关系如图 4所示。 .另取两个密闭容器,分别装入 20g硅胶和 20g氯化钙,测得时间与相对湿度变化 关系如图 5 所示。 (4)图 4的曲线表征,可以推测密闭容器甲的湿度增大的原因是_(从微观角度 解释)。 (5)根据图 5的数据分析,干燥剂吸收水分的效果与_有关,在单位时间内干 燥效果较好的是_。 (6)请设计实验探究:干燥剂的干燥效果是否与温度有关_。 【反思交流】 (7)生活用品中常用硅胶或氯化钙等做干
12、燥剂, 而不用浓硫酸的主要原因是_。 第 7 页,共 13 页 答案和解析答案和解析 1.【答案】A 【解析】解:A、粮食酿酒,酒精是新物质,属于化学变化;故选项正确; B、纸张粉碎没有新物质生成,属于物理变化;故选项错误; C、衣服晒干没有新物质生成,属于物理变化;故选项错误; D、石蜡熔化没有新物质生成,属于物理变化;故选项错误; 故选:A。 有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化,纸张粉碎、衣服 晒干、石蜡熔化都属于物理变化。化学变化的特征是:有新物质生成。判断物理变化和 化学变化的依据是:是否有新物质生成。 本考点考查了物理变化和化学变化的区别,基础性比较强,只要
13、抓住关键点:是否有新 物质生成,问题就很容易解决。本考点主要出现在选择题和填空题中。 2.【答案】D 【解析】解:A、洗洁精洗油污是利用了乳化原理,故 A说法正确; B、小苏打和柠檬酸反应生成二氧化碳,可以用来自制汽水,故 B 说法正确; C、电器着火的灭火方法:先切断电源再灭火,故 C说法正确; D、霉变大米中含有致癌物,不能再食用,故 D 说法错误。 故选:D。 A、根据洗洁精洗油污的原理考虑; B、根据小苏打和柠檬酸反应生成二氧化碳考虑; C、根据电器着火的灭火方法考虑; D、根据霉变大米不能再食用考虑。 解答本题关键是熟悉洗洁精洗油污的原理,灭火的方法,霉变食物的危害。 3.【答案】C
14、 【解析】解:信州铅山胆水自山下注,势若瀑布,用以浸铜古传一人至水滨,遗匙 钥, 翌日得之, 已成铜矣, 即生成了铜, 则这里的胆水指的是铜盐的水溶液, 指的是4 溶液。 故选:C。 根据题意, 信州铅山胆水自山下注, 势若瀑布, 用以浸铜古传一人至水滨, 遗匙钥, 翌日得之,已成铜矣,即生成了铜,进行分析判断。 本题难度不大,明确已成铜矣的含义(说明生成了铜)是正确解答本题的关键。 4.【答案】D 【解析】解:A、复合轻钢板材是由多种材料制成,所以属于复合材料,故 A正确; B、医院对污染的废弃物直接无害化处理,可以防止污染环境,故 B正确; C、紫外线消毒系统,可以有效杀死病毒,故 C正确
15、; D、聚乙烯膜是由聚乙烯制成的,聚乙烯属于有机合成材料,故 D错误。 故选:D。 A、根据复合轻钢板材是由多种材料制成进行解答; B、根据医院对污染的废弃物直接无害化处理,可以防止污染环境进行解答; C、根据紫外线消毒系统,可以有效杀死病毒进行解答; D、根据聚乙烯膜是由聚乙烯制成的进行解答。 解答本题关键是熟悉常见材料的分类,属于基础知识的考查,难度较小。 第 8 页,共 13 页 5.【答案】B 【解析】解:.镁在空气中燃烧生成氧化镁,部分氧化镁扩散到空气中而造成污染,不 合题意; B.硫在氧气中燃烧生成的二氧化硫溶于水或被氢氧化钠溶液吸收, 没有扩散到空气中造 成污染,符合题意; C.
16、硫酸铵与熟石灰反应生成有刺激性气味的氨气扩散到空气中而造成污染,不合题意; D.铜片上的白磷燃烧生成的五氧化二磷有毒,扩散到空气会造成污染,不合题意。 故选:B。 根据化学反应的产物以及造成空气污染的物质来分析。 本题考查了反应的产物以及造成空气污染的物质,难度不大。 6.【答案】C 【解析】解:A、面粉溶于水形成的悬浊液,而不是溶液,故 A 错误; B、氧化铝、氧化镁是白色固体,而不是黑色固体,故 B 错误; C、煤、石油、天然气都属于化石燃料,故 C 正确; D、铁、锌都是人体需要的微量元素,钙属于常量元素,故 D错误。 故选:C。 A、根据面粉溶于水形成的悬浊液进行解答; B、根据氧化铝
17、、氧化镁是白色固体进行解答; C、根据常见的化石燃料进行解答; D、根据人体常见的微粒元素进行解答。 解答本题关键是熟悉物质的水溶性、化石燃料以及物质的性质,属于基础知识的考查, 难度较小。 7.【答案】B 【解析】解:A、W 点所示物质为硫,可以通过与氧气之间的化合反应生成 X点所示物 质二氧化硫,故选项正确; B、X点所示物质二氧化硫中硫元素和氧元素的质量比为 32:(16 2) = 1:1,故选项 正错误; C、Y点所示物质是硫酸,可用于金属除锈,故选项正确; D、Z点所示物质属于硫酸盐,可以为24故选项正确。 故选:B。 根据硫元素的化合价确定物质的类别,从而得到相应物质的化学式。 本


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 福建省 莆田市 2020 年中 化学 试卷 答案 解析
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-142829.html