 2019年内蒙古包头市中考化学试题(含答案)
2019年内蒙古包头市中考化学试题(含答案)
《2019年内蒙古包头市中考化学试题(含答案)》由会员分享,可在线阅读,更多相关《2019年内蒙古包头市中考化学试题(含答案)(6页珍藏版)》请在七七文库上搜索。
1、2019 内蒙古包头市中考化学部分内蒙古包头市中考化学部分 化学(化学(40 分)分) 可能用到的相对原子质量:可能用到的相对原子质量: H-1 C-12 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 K-39 Ca-40 Mn-55 Fe-56 Cu-64 Zn-65 Ag-108 一、选择题(本题包括一、选择题(本题包括 6 个小题,每小题个小题,每小题 2 分,共分,共 12 分。每小题只有一个选项符合题意,分。每小题只有一个选项符合题意, 请将答题卡上对应题目的答案标号涂黑)请将答题卡上对应题目的答案标号涂黑) 1.(2019包头)下列变化是化学变化的是( )
2、 A.海水晒盐 B.铁丝燃烧 C.石墨导电 D.干冰升华 【答案答案】B 【解析】【解析】铁丝燃烧生成四氧化三铁,有新物质生成,是化学变化。 2. (2019包头)下列做法合理的是( ) A.发现家中天然气泄漏,立即打开抽油烟机 B.为治理雾霾,禁止使用化石燃料 C.为防止废旧电池污染环境,把电池深埋地下 D.在汽油中加入适量乙醇作为汽车燃料,可减少对环境的污染 【答案答案】D 【解析】【解析】打开抽油烟机通电会产生电火花,天然气具有可燃性,遇电火花易生爆炸;现今还 没有比较好的能源能全部代替化石燃料,只能少用而不能禁止;旧电池内藏着汞、铅等重金 属, 这些重金属进入人体会危害人的健康; 乙醇
3、和普通汽油按一定比例混配形成的新型替代 能源,可减少化石燃料的使用,减少环境污染。 3. (2019包头)下列叙述正确的是( ) A.有单质和化合物生成的反应不一定是置换反应 B.pH 大于 7 的溶液一定是碱溶液 C.不同种元素组成的物质都是化合物 D.电解水实验表明:水是由两个氢原子和一个氧原子构成的 【答案答案】A 【解析】【解析】 不是有单质和化合物生成的反应就是置换反应, 如 2H2O2二氧化锰 2 H2O+O2是分 解反应;pH7 的溶液一定显碱性,但不一定是碱溶液,如碳酸钠溶液是盐的溶液但显碱性; 化合物是由两种或两种以上元素组成的纯净物, 不同种元素组成的物质有可能是混合物,
4、不 一定是化合物; 电解水的实验说明水是由氧元素和氢元素组成, 一个水分子是由两个氢原子 和一个氧原子构成的。 4. (2019包头)下列实验能够达到目的是( ) A.除去 KNO3溶液中混有的 K2SO4,加入适量的 BaCl2溶液,过滤 B.制备 Cu(OH)2,可将 Ba(OH)2溶液和适量 CuSO4溶液混合,过滤 C.鉴别 NaOH、NaCl、CuSO4和稀盐酸四种溶液,不需添加任何试剂就可完成 D.分离 NaCl 和 MgCl2的固体,先加水溶解,再加入适量的 NaOH 溶液过滤,向滤渣滴加适量 稀盐酸 【答案答案】C 【解析】【解析】 硫酸钾与氯化钡反应生成硫酸钡沉淀和氯化钾,
5、经过过滤仍然引入了新杂质氯化钾; 氢氧化钡与硫酸铜反应生成硫酸钡与氢氧化铜两种沉淀, 不能得到纯净的氢氧化铜; 硫酸铜 溶液是蓝色的,能与硫酸铜溶液反应产生蓝色沉淀的是 NaOH,再将剩余的两种溶液分别滴 加至蓝色沉淀中,能使沉淀消失的是稀盐酸,无明显变化的是氯化钠,不加入试剂能够鉴别 以上四种物质;NaCl 和 MgCl2的固体混合物,溶解,加适量 NaOH,生成氢氧化镁沉淀和氯 化钠,过滤,向滤渣中滴加适量稀盐酸,氢氧化镁与稀盐酸反应生成氯化镁和水,能进行分 离,但不能得到氯化钠和氯化镁固体。 5. (2019包头)盛有等质量、等质量分数稀盐酸的两只烧杯,放在托盘天平的左右两盘, 天平平衡
6、。在左盘烧杯中加入 10 gCaCO3恰好完全反应。若要使天平重新平衡,则右盘烧杯 中应加入的下列物质是( ) A.5.6g 铁和锌 B.10g 镁和氧化镁 C.10g 碳酸镁 D.10g 碳酸钠和碳酸锌 【答案答案】C 【解析】【解析】铁和锌均能与盐酸反应放出氢气,因只加入 5.6g 铁和锌,将放出氢气减掉,实际 右盘增加少于 5.6g;向右盘加入 10g 镁和氧化镁,若 10g 全是氧化镁,因反应无气体放出, 右盘增量为 10g,若 10g 全是镁,则盐酸全部反应,没有剩余,产生 0.2g 氢气,实际右盘增 加 10g-0.2g=9.8g;10gMgCO3与 7.3g 盐酸反应,碳酸镁有剩
7、,生成二氧化碳 4.4g,实际上相 当于右盘增重 10g-4.4g=5.6g;因碳酸钠和碳酸锌的平均分子质量应该在 106 和 125 之间, 10g 碳酸钠和碳酸锌与 7.3g 盐酸反应,盐酸有剩余,生成二氧化碳质量少于 4.4g,其实际右 盘增加大于 5.6g。 6.(2019包头)下表中,有关量的变化图像与其对应叙述相符的是( ) A B C D 向一定质量的稀硫酸 中加入足量的铁 向一定质量的氢氧 化钠溶液中加入稀盐 酸 向等质量、 等质量分 数的稀盐酸中加入足 量的铁和铝 加热高锰酸钾固体制 氧气 【答案】B 【解析】向一定质量的稀硫酸中加入足量的铁,反应前有一定质量的稀硫酸,坐标图
8、的起点 溶液质量不为 0;向一定质量的氢氧化钠溶液中加入稀盐酸,反应前有一定质量的氢氧化钠 溶液,溶剂质量不为 0,加入稀盐酸发生反应,增加溶剂质量包括反应物稀盐酸中的水和反 应生成的水,当 NaOH 反应完,继续加入稀盐酸,增加溶剂质量只是稀盐酸中的水,所以加 入稀盐酸的整个过程溶剂质量增大,且先增幅较大后增幅较小;向等质量、等质量分数的稀 盐酸中,分别加入足量的镁和铝,消耗金属质量镁大于铝,生成的氢气质量相等;加热高锰 酸钾,固体生成物有 K2MnO4 和 MnO2,含氧元素,反应后固体中含有氧元素质量不为零。 二、填空题(本题包括二、填空题(本题包括 4 个小题,化学方程式个小题,化学方
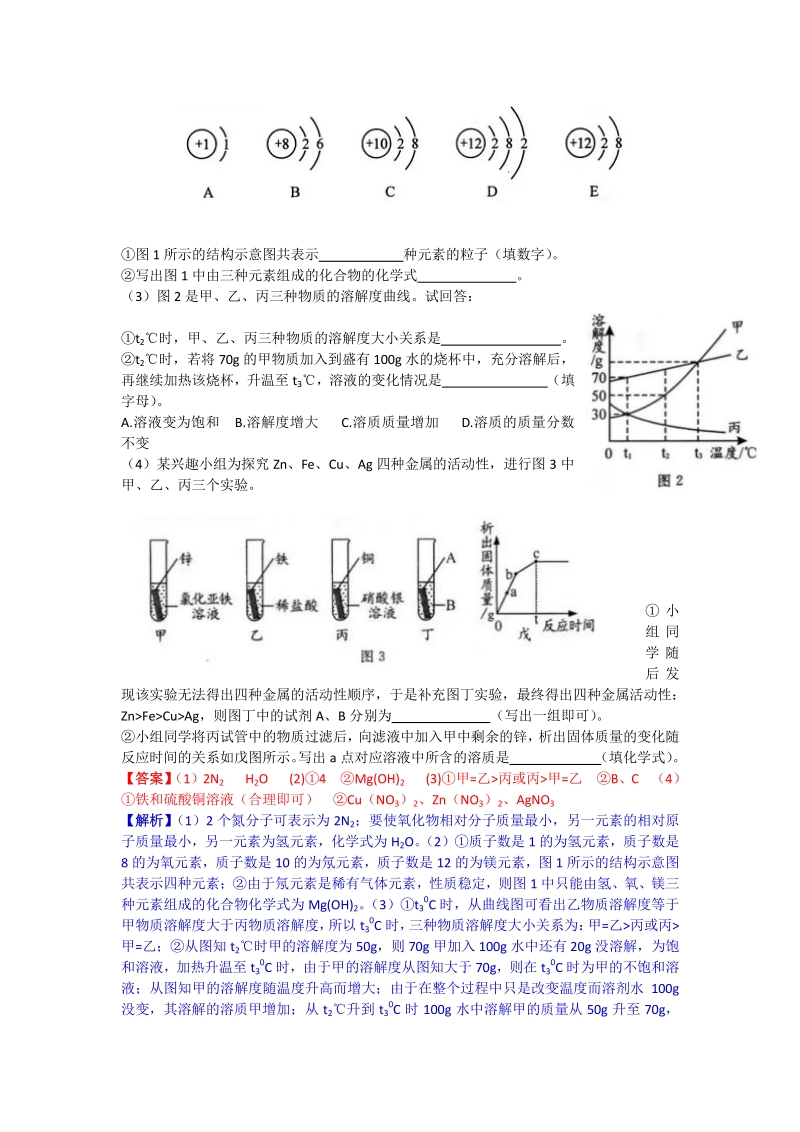
9、程式 2 分,其余的每空分,其余的每空 1 分,共分,共 21 分。请将答案分。请将答案 写在答题卡的对应位置)写在答题卡的对应位置) 7. (2019包头) (1)用化学符号填空: 2 个氮分子 ;相对原子质量最小的氧化物 。 (2)根据图 1 回答: 图 1 所示的结构示意图共表示 种元素的粒子(填数字) 。 写出图 1 中由三种元素组成的化合物的化学式 。 (3)图 2 是甲、乙、丙三种物质的溶解度曲线。试回答: t2时,甲、乙、丙三种物质的溶解度大小关系是 。 t2时,若将 70g 的甲物质加入到盛有 100g 水的烧杯中,充分溶解后, 再继续加热该烧杯,升温至 t3,溶液的变化情况是
10、 (填 字母) 。 A.溶液变为饱和 B.溶解度增大 C.溶质质量增加 D.溶质的质量分数 不变 (4)某兴趣小组为探究 Zn、Fe、Cu、Ag 四种金属的活动性,进行图 3 中 甲、乙、丙三个实验。 小 组 同 学 随 后 发 现该实验无法得出四种金属的活动性顺序,于是补充图丁实验,最终得出四种金属活动性: ZnFeCuAg,则图丁中的试剂 A、B 分别为 (写出一组即可) 。 小组同学将丙试管中的物质过滤后, 向滤液中加入甲中剩余的锌, 析出固体质量的变化随 反应时间的关系如戊图所示。 写出 a 点对应溶液中所含的溶质是 (填化学式) 。 【答案答案】 (1)2N2 H2O (2)4 Mg


- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 2019 年内 蒙古 包头市 中考 化学试题 解析
 七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
七七文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。



 浙公网安备33030202001339号
浙公网安备33030202001339号
链接地址:https://www.77wenku.com/p-136794.html